Фармакодинамика
СОДЕРЖАНИЕ: Фармакодинамика как один из фундаментальных разделов фармакологии. Различие главного и побочного действия лекарств. Роль ионных связей в механизме действия лекарств. Определение терапевтического индекса. Влияние внешних факторов на реакцию лекарства.Реферат
ПО ФАРМАКОЛОГИИ
НА ТЕМУ: ФАРМАКОДИНАМИКА
Одним из фундаментальных разделов фармакологии является фармакодинамика, занимающаяся изучением изменений, происходящих в организме под действием лекарств. За некоторым исключением действие лекарственных веществ включает взаимодействие его с клеткой, ее субклеточными структурами (лизосомы, митохондрии), мембранами, ферментами, нуклеиновыми кислотами и некоторыми другими специальными клеточными и экстрацеллюлярными биологическими субстратами. В зависимости от функциональной роли клетки реакция может быть местной или генерализованной, захватывающей многие процессы. В зависимости от места применения и всасывания в кровь различают местное и резорбтивное действие лекарственных средств. В свою очередь резорбтивное действие может быть обусловлено прямым или непрямым влиянием вещества на эффектор. Например, вещество может расширять кровеносные сосуды действием на гладкие мышцы сосудов (прямое действие) или воздействием на холодовые рецепторы (непрямое, или косвенное, действие). Рефлекторное действие является одним из вариантов косвенного. Механизм его заключается во взаимодействии лекарства с окончаниями чувствительных нервов; возникающий импульс по соответствующие рефлекторным дугам передается к эффекторным органам (действие раздражающих, отхаркивающих и др.),
Специфика структур-рецепторов определяет избирательное действие фармакологического агента, сущность которого заключается в том, что первичная фармакологическая реалия может произойти только в данной группе клеток. Однако специфическое, или избирательное, действие не является абсолютным, поскольку лекарства могут реагировать с разными субстратами цитоплазмы, поэтому правильнее говорить о преимущественном действии холинолитиков, адреиомиметиков и др. Если вещество не оказывает прямого влияния на строго определенные рецепторы, его действие называют неспецифическим (ингаляционные наркотики, детергенты). В структуре таких лекарств не выделяются фармакофорные радикалы, а их физиологическая активность больше коррелирует с размером молекулы, растворимостью в неполярных растворителях и т. д. Многие из неспецифически действующих агентов (соли тяжелых металлов, хинин) угнетают функцию любой живой клетки; их относят к средствам общеклеточного действия, или к про-топлазматическим ядам.
С клинической точки зрения следует различать главное и побочное действие лекарств. Действие, с помощью которого достигается терапевтический эффект, является главным, все же остальные фармакологические реакции — побочными явлениями. В зависимости от целей лечения главное и побочное действия могут меняться ролями. Так, при лечении язвенной болезни атропином главное действие — снижение двигательной активности и секреции желез пищеварительного аппарата, побочное — расширение зрачков и паралич аккомодации, в офтальмологии — наоборот. К отрицательным побочным явлениям относятся: токсическое действие, обусловленное повышенной чувствительностью организма, лекарственные аллергические реакции, эмбриотоксическое, тератогенное, мутагенное, бластомогоное действие. Особый вид извращенных реакций — идиосинкразия, обусловленная наследственным дефицитом обезвреживающих ферментов. Еслы побочные явления становятся доминирующими и угрожают жизни больного (например, аллергия при пенициллинотерапии агранулоцитоз при применении амидопирина или сульфаниламидов и др.)» лечение следует отменить или назначить менее опасный препарат.
Как в клинической, так и экспериментальной медицине существует понятие «обратимое действие», когда после фармакологического воздействия восстанавливается деятельность органа или организма (например, пробуждение после наркоза). Необратимое действие лекарства обусловлено деструкцией клеток и тканей. Таким действием обладают средства против бородавок, мозолей опухолевой ткани. Действие почти всех лекарств втоксических дозах необратимо.
Реакция ксенобиотика с биологическим субстратом-лигандом может осуществляться при помощи физических, физико-химических и химических взаимодействий. Редко эффект лекарства обусловлен каким-либо одним характером взаимодействия, например вещество А может адсорбироваться на поверхности белковой молекулы, растворяться в липидной части мембраны и тем самым изменять состояние клетки. Физические физико-химические реакции присущи тем из лекарств, которые выделяются из организма в неизмененном и малоизмененном виде (инертные газы, азот и др.). Большинство ксенобиотиков подвергаются в организме химическим превращениям, поэтому их действие в основном обусловлено способностью образовывать различные химические связи с мишенями. Некоторые вещества, в частности алкилирующие агенты, образуют с биологическими субстратами ковалентные связи; действие таких веществ необратимо. Важное значение имеет образование координационных ковалентных связей, довольно распространенных в живой природе. Лекарства и антидоты, способные образовывать стабильные комплексы (циклические системы), называют хелатными комплексами (например, комплекс унитиола с мышьяком или тистацин-кальция со свинцом).
Определенную роль в механизме действия лекарств играют ионные связи; они гораздо слабее ковалентных и возникают в тех случаях, когда лекарства содержат катионную или анионную группу, а противоположные структуры находятся в биологических лигандах. Действие лекарства в подобных случаях носит обратимый характер. Часто ионные связи образуются на первых ступенях фармакологической реакции между ксенобиотиками и рецепторами.
Связи, возникающие в результате дипольных взаимодействий, на» называются водородными. Обычно они имеются в молекулах, где атом водорода ковалентпо связан с другим электроотрицательным атомом. Водородные связи обеспечивают поддержание стабильности двойной спирали ДНК И вторичные структуры белков, лежат в основе сократимости. Для них характерен эффект кооперативное водородных связей, когда энергия суммы водородных связей с увеличением числа отдельных связей возрйтает.
Понятно, что ксенобиотик, встраиваясь в биологические структуры, существенно изменяет их функцию. Кроме того, водородные связи участвуют в процессах узнавания и фиксации лекарства к физиологически важным структурам.
Самые слабые силы взаимодействия, возникающие между, лекарствами и биологическим лигандом, вандервальсовые, обусловлены дипольными взаимодействиями. В реакции ксенобиотика с биологическим субстратом они имеют меньшее значение, чем ковалентные связи, но принимают участие в определении специфичности взаимодействия вещества с биохимическими реактивными системами.
Кроме того, существует гидрофобное взаимодействие. Хотя энергия его связей мала, взаимодействие большого числа длинных алифатических цепей приводит к возникновению стабильных систем. Гидрофобные взаимодействия играют определенную роль в стабилизации конформаций биополимеров и образовании биологических мембран. В свою очередь ксенобиотик, обладающий способностью образовывать гидрофобные связи, нарушает структуру мембран, а следовательно, и соответствующие биохимические и биофизические процессы. В фармакологической реакции важное значение имеет среда, соответствующие составные части которой в значительной степени могут моделировать конечный эффект.
Большинство органических соединений представляют собой сложные структуры, содержащие различные по реакционной способности радикалы и имеющие многомерную объемную форму. Благодаря участию большинства перечисленных сил они могут избирательно связываться с биологическими лигандами. Фармакологическая активность зависит от структурной и пространственной изомерии. Пространственная изомерия в свою очередь делится на виды: оптический, геометрический. Кроме того, как молекула лекарства, так и биологическая структура способны менять свою форму, становясь комплементарными друг к другу. Иными словами, пространственные функциональные группы действующего вещества могут адаптироваться к активным центрам — макромолекулам биосубстрата, в связи с чем облегчается образование перечисленных связей.
Этим можно объяснить фармакологический парадокс, заключающийся в высокой избирательности и большой биологической активности малореактивных в химическом отношении молекул. Фармакологические связи схематически представлены на рис. 8.
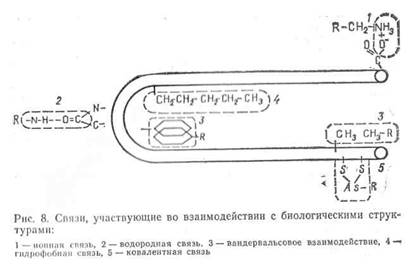
Естественно, действие лекарств интимно связано с их химической структурой, физико-химическими свойствами. Взаимоотношения эти довольно специфичны, поскольку для изменения фармакологической активности вещества иногда достаточно небольших изменений в молекуле. Изучение зависимости между структурой, физико-химическими свойствами соединения и его действием на организм позволяет целенаправленно синтезировать новые более активные и менее токсичные соединения и глубже понять механизм их действия. Кроме того, на основе физико-химических свойств моделируются лекарственные формы и биодоступность.
Лекарство, поступив в организм, в зависимости от строения и физико-химических свойств, может взаимодействовать с любыми его •составными частями и даже с водой. Однако в процессе эволюции многоклеточных организмов выработались вещества и специальные клеточные структуры, обеспечивающие оптимизацию гомеостаза к постоянно меняющимся условиям внешней среды. Именно благодаря молекулярным особенностям протоплазмы в различных клетках под влиянием введенного вещества возможны специфические изменения в одних клетках и полное отсутствие реакции в других. Эти специфические вещества называются медиаторами, а структуры, с которыми они взаимодействуют,— рецепторными субстанциями, или рецепторами. За последние десятилетия наиболее интенсивно изучались адрено-, холино-, серо-тонино-, гистаминореактивные системы, многие другие медиаторы и их рецепторы. Показано, что процессы медиаций носят каскадный характер, начиная от синтеза медиатора, его депонирования, освобождения, обратного захвата до взаимодействия с рецепторами и разрушения. На этой основе создано много веществ, фармакологически регулирующих перечисленные процессы и являющихся эффективными лекарствами. Созданы как агонисты, действующие однонаправленно, так и антагонисты, действующие в противоположных направлениях.
Фармакологические агенты связываются помимо рецепторов, с которыми обусловлено специфическое действие, еще со многими макромолекулами, например с белками плазмы, с белками клеток, с ферментами, осуществляющими биотрансформацию ксенобиотика. Подобные места связывания называются вторичными, или молчащими, рецепторами местами потери, или местами депонирования, или акцепторами лекарств.
В многоступенчатом механизме действия лекарств можно условно выделить: 1) фармакокинетику—всасывание, распределение, превращение и выделение; 2) взаимодействие вещества с рецептором и порождение им стимула; 3) процессы, определяющие отношение между вызванным импульсом и регистрируемым эффектом. Известно, что между силой импульса и величиной эффекта в одних случаях может существовать корреляционная зависимость до достижения максимальных величин, в других случаях эффект может возникать по принципу «все или ничего».
Современные рецепторные теории базируются на том, что все рецепторы равноценны, одинаково доступны и способны взаимодействовать с веществом, а эффект пропорционален числу занятых рецепторов. Согласно одной из простейших теорий, так называемой теории занятости, считается, что организм имеет фиксированное число, по-видимому, независимых эквивалентных рецепторов. По теории занятости, дифференцированный отклик пропорционален доле рецепторных полей, занятых молекулами препарата. Следовательно, максимальный эффект достигается, когда все рецепторы заняты; в таких случаях математически все явления можно описать кинетическим уравнением Михаэлиса—Ментен.
По теории занятости, вещества действуют все время, пока они Находятся на рецепториом участке. Согласно другой точке зрения, воздействие/ осуществляется только в момент связывания препарата с рецептором (за счет конформациониых изменений рецептора), как в случае появления импульсного потенциала действия, сопровождающего перенос нейромедиатора на рецепторе постсинастической мембраны. Эта модель лежит в основе теории скоростей взаимодействия лекарств с рецепторами. Уравнение теории скоростей описывает ту же самую функциональную связь между эффектом и дозой, что и уравнение Михаэлиса—Ментен.
В результате количественного анализа перечисленных теоретических предпосылок возникло представление, что эффект лекарства определяется не только способностью образовывать комплекс вещество — рецептор, обусловленной сродством или аффинитетом вещества к рецептору, но и возможностью активации последнего. Действенность самого процесса взаимодействия лекарства с рецептором принято обозначать как внутреннюю активность, или эффективность.
Аффинитет и внутренняя активность фармакологических средств являются выражением химической структуры веществ, их физико-хими-ческих свойств, но проявляются они только во взаимодействии с рецепторной структурой.
В результате развития рецепторной теории на основе изучения роли циклических нуклеотидов, в частности циклической АМФ, ГМФ и др., в последние появилось представление о вторичных передатчиках. Их роль можно проследить на примере увеличения адреналином фосфорилазной активности. Адреналин повышает фосфорилазную активность, стимулирует фермент аденилатциклазу, которая увеличивает синтез циклдаеской АМФ, а последняя активирует фосфорилазу. Доказано, что в действии многих медиаторов, гормонов и лекарственных веществ принимают участие циклические нуклеотиды.
Конечно, все многообразие действия лекарств не исчерпывается рецепторным взаимодействием. Существует множество других механизмов — химических, физических, биохимических, биофизических и др. Многие вещества непосредственно реагируют с токсинами: унитиол и ЭДТА с солями тяжелых металлов образуют стабильные комплексы и таким образом реактивируют жизненно важные ферменты, ионно-обменные смолы; антациды при приеме внутрь нейтрализуют кислоту в желудке; под воздействием аммония хлорида увеличивается количество ионов водорода и повышается содержание кислых продуктов в моче. Натриевые соли органических и угольной крови повышав щелочной резерв крови и повышают pН мочи·. Детергенты разрушают целостность липидной мембраны и нуклеопротсидные комплексы рибосом. Галоиды, окиси и перекиси в результате пёрекионогф окисления вызывают изменение структуры мембран. Денатурирующие вещества (фенолы, соли тяжелых металлов) нарушают целое гость и функциональные свойства клеточных мембран, субклеточных структур и белков. Действие летучих наркотиков обусловлено их способностью растворяться в липоидах мембран нейронов и нарушать их функции кроме того, имеются данные , что инертные газы могут изменять «кристаллическое состояние воды» и тем самым оказывать наркотическое действие. Магния сульфат дает слабительный эффект; мочевина и маннитол — мочегонное действие, благодаря изменению осмотического давления, Регуляция осмотического давления лежит в основе действия кровезаменителей. Существенное значение в фармакодинамике имеет блокада даШчёвых ферментов (холинэстеразы, цитохромоксидазы), сложных биоэнергетических процессов, разобщение окислительного фосфорилирова-ния, транспорта ионов, нарушение синтетических процессов с использованием антиметаболитов.
Все вышеперечисленные количественные и качественные процессы входят в понятие первичной фармакологической реакции. Обычно она протекает скрыто и проявляется в виде клинически диагностируемых реакций организма или, как их принято называть, фармакологических эффектов, обусловленных физиологическими свойствами клеток, органон и систем. Например, ацетилхолии вызывает сокращение гладких мышц бронхов, пищеварительного аппарата, увеличивает секрецию слюнных желез. Однако в основе однотипных фармакологических эффектов могут быть разные первичные фармакологические реакции. Так, ангиотензин и норадреналин вызывают сокращение гладких мышц сосудов, но эффект ангиотензина обусловлен непосредственным влиянием на последние и повышением выброса норадреналина, торможением его обратного захвата и повышением чувствительности адренорецепторов, тогда как эффект норадреналина — взаимодействием его с альфа-адренорецепторами сосудистой стенки;
Обычно под воздействием лекарств (антикоагулянты, сосудорасширяющие вещества, анальгезирующие и др.) происходят биохимические и физиологические изменении, врезультате исчезают клинические симптомы, Однако для Количественной и сравнительной характеристики приходится прибегать к таким понятиям, как максимальный эффект, его вариабельность и избирательность. Важна характеристика эффекта во времени как при приеме однократной дозы, так и после повторных приемов препарата. Каждый эффект лекарства, как правило, по времени можно разделить на латентный период, время максимального лечебного эффекта и его продолжительность.
Каждый из этапов обусловлен рядом биологических процессов. Так, латентный период определяется в основном путем введения, скоростью всасывания и распределения вещества по органам и тканям, в меньшей степени — его скоростью биотрансформации и экскреции. Продолжительность эффекта обусловлена преимущественно скоростью инактивации и выделения. Определенное значение имеют перераспределение действующего агента между местами действия и депонирования, фармакологические реакции и развитие толерантности. В большинстве случаев с увеличением дозы лекарства уменьшается латентный период, увеличиваются эффект и его продолжительность. Удобно и практически важно выражать продолжительность лечебного действия полупериодом снижения эффекта. Если полупериод совпадает с концентрацией вещества в плазме, врач получает объективный критерий для контроля и направленной регуляции терапевтической активности. Другой критерий — полупериод нарастания концентрации и эффективности — можно использовать для характеристики процессов биодоступности, всасывания, распределения лекарства, между органами и тканями . Как уже отмечалось, эффективность лекарства зависит от его дозы. Большая корреляция определяется между концентрацией и эффектом. Однако на практике прямая зависимость между концентрацией вещества в сыворотке и величиной эффекта наблюдается очень редко в связи с многокаскадностью лежащих в основе взаимодействия лекарств и организма процессов. Так, снижение или повышение артериального давления может быть результатом изменения сердечной деятельности, тонуса сосудов, объема циркулирующей крови и нервной регуляции, а также одновременных или последовательных их сочетаний. В связи с этим кривая может быть прямой, изогнутой вверх или вниз, сигмой-дального характера. Если все же вычленить какой-то один компонент, то кривая доза — эффект приобретает строго определенный характер с параметрами, отражающими силу, наклон и максимальную эффективность.
По расположению кривой доза — эффект относительно оси доз можно судить о силе действия лекарства, всех фармакокинетических показателях (всасывание, распределение, превращение и выделение), а также о сродстве лекарства с рецепторами. Для сравнения силы действия двух и более средств используют относительную силу их действия — определение эквиэффективных доз. Характер подъема в какой-то степени характеризует механизм действия вещества, а максимальный эффект — внутреннюю активность лекарства. Анализ кривых доза — эффект морфина и кислоты ацетилсалициловой убедительно показывает, что морфин имеет достаточную внутреннюю активность, чтобы снять сильную и слабую боль, в то время как кислота ацетилсалициловая даже в максимальных дозах может без проявления токсических свойств снять лишь болевой синдром средней тяжести.
Клиническая практика показывает, что величина эффекта строго индивидуальна. Кривую доза — эффект можно получить в строго контролируемых условиях или вывести среднюю величину на основании кривых многих больных. Для сравнительной оценки лекарств прибегают к таким понятиям, .как средняя эффективная, доза (ЕД50)—доза лекарства, необходимая для получения эффекта определенной интенсивности у 50 % пациентов). Явление повышенной чувствительности к малым дозам обозначается как гиперреактивность. Нельзя использовать в этих случаях понятие «гиперчувствительность», характеризующее лекарственную аллергию. Сверх или суперчувствительность, характерна для денервированпых органов. Если больной слабо реагирует на большие дозы вещества, говорят о гипореактивности. Гипореактивность иногда отождествляют с толерантностью, однако это не совсем правильно, так как толерантность возникает лишь после повторного введения вещества. Толерантность, развивающаяся очень быстро при введенийНескольких доз лекарства, определяют как тахифилаксию. В тех случаях, когда в основе гипореактивпости лежит выработка антител^ говорят об иммунитете. Необычная реакция организма на некоторые пищевые продукты и лекарства, возникающая у людей с наследственно обусловленной повышенной чувствительностью к ним и похожая по клиническим проявлениям на аллергическую, называется идиосинкра-вией. Лекарственная идиосинкразия чаще всего проявляется чрезвычайной чувствительностью к малым дозам лекарств, которые дают эффект, Или появлением различных изменений в системах, на которые действие лекарственного препарата не направлено; некоторые авторы относят к идиосинкразии также случаи очень низкого терапевтического, эффекта от доз, превосходящих терапевтические. В основе идиосинкразии, согласно современным представлениям, лежит генетически обусловленный недостаток определенных ферментов, участвующих в метаболизме лекарственных средств.
Кроме толерантности (привыкание, резистентность) и тахифилаксии, при повторном введении лекарств могут наблюдаться явления химической, или функциональной, кумуляции, обусловленной в одних случаях накоплением вещества (сердечные гликозиды, соли тяжелых металлов, стрихнин, ДДТ и др.), в других — суммированием эффектов (коразол). В некоторых случаях при применении веществ, влияющих па психический статус, вызывающих эйфорию (морфин, алкоголь, ко каин и др.), развивается пристрастие, или лекарственная зависимость. После применения химиотерапевтических средств возможны такие осложнения, как дисбактериоз, и реакции, обусловленные гибелью большого количества бактерий.
Очень важной стороной фармакодинамики является избирательность, или селективность, действия. Обычно, когда говорят о действии лекарства, имеют в виду основной его эффект. Например, морфин—· болеутоляющее средство; кроме того, он угнетает дыхание, кашлевой рефлекс, вызывает сонливость, эйфорию, запор, сужение зрачков и т. д. Поэтому правильнее говорить о фармакологическом спектре действия лекарства, а для определения безвредности использовать интегральные показатели, В этих случаях приходится прибегать к таким количественным понятиям, как терапевтический индекс, границы безопасности, которые отражают соотношение между желательным и нежелательным действием лекарства. Конечно, если бы лекарство обладало только основным видом активности и не давало побочных отрицательных явлений, то можно было бы ограничиться расчетом отношения минимально токсической к минимально эффективной дозе. Практически минимальные эффективные дозы определить очень трудно, поэтому приходится использовать среднетоксичние и среднеэфективные дозы. Терапевтический индекс определяют экспериментально по формуле:
![]()
где — терапевтический индекс, LD50 — доза вещества, вызывающая гибель половины животных, ЕД50 — доза или концентрация вещества,
дающая эффект 50 % от максимального при градированных реакциях, а при альтернативных — у 50% исследуемых., Затем экстраполируют полученные данные на больного,
В клинике избирательность приходится определять косвенным путем. Суммируются все случаи побочных явлений; в том числе вынуждавших отменять лечение, и выражаются в процентах ко всем больным, леченным данным препаратом. Более приближенной к клиническим условиям величиной является отношение дозы, которая вызывает токсический эффект у ! % больных и лечебный у 99 %, что может быть выражено как![]() в опытах на животных. В клинике вместо
в опытах на животных. В клинике вместо
LD используют токсические дозы LD1/ЕД99. Например, для дигитоксина доза, уменьшающая частоту возникновения фибрилляции предсердий вдвое, является критерием терапевтического действия, а появление рвоты свидетельствует о том, что доза лекарства является токсической. В частности, доза дигитоксина, дающая эффект у 99 %, вызывает рвоту у 3 % больных, поэтому при лечении препаратами дигиталиса необходим индивидуальный подход.
К сожалению, токсические (побочные) явления (головная боль, тошнота) иногда обнаруживаются в клинике после длительного применения лекарства (например, левомицетина) и вовсе не моделируются в эксперименте, что создает большие трудности для их прогнозирования и предотвращения.
Действие лекарства на организм, т. е. фармакологический эффект,
зависит как от химической структуры, физико-химических свойств вещества, так и от особенностей организма и внешней среды, в которой происходит действие данного лекарства. Изменение в ту или иную сторону реакции организма на лекарство может носить групповой, качественный характер. Например, при сенсибилизации организма и появлении аллергических реакций или изменении иммунного статуса такие реакции трудно· прогнозировать; в каждом случае требуется предварительное испытание на больном. Другая часть реакций носит количественный характер и строго специфична для данного лекарства, что следует учитывать при назначении лечения. Конечно, снижение терапевтического эффекта может быть результатом колебаний фармакологических показателей или фармакодинамики. При некоторых видах патологии вычленить фармакокинетические сдвиги довольно легко. Так, при патологии почек нарушается экскреция, при болезнях печени — био
трансформация лекарств, в результате чего действие их усиливается,
но и в этих случаях трудно исключить (иногда очень слабый) фармакодинамический компонент. В связи с этим обычно приходится ориентироваться на суммарные результаты — увеличение или уменьшение реакции организма на лекарство.
Обычно между гомеостазом организма и окружающей средой устанавливается динамическое равновесие, нарушение которого существенно отражается на реактивности организма. Действие лекарств при нарушении равновесия также соответственно моделируется, что необходимо учитывать в эксперименте и клинической практике. Только накопление достаточного количества данных о влиянии факторов окружающей среды на фармакологические эффекты дает возможность регулировать силу воздействия этих факторов на больного и позволяет, проводить по-настоящему рациональную фармакотерапию.
Условно эффекты внешней среды можно разделить на внешние и внутренние. Под внешними понимают изменение внешней среды во время взаимодействия лекарства с организмом (температура, радиация, звук, вибрация, состав воздуха, атмосферное давление, влажность, вода; пища, социальные или зоосоциальные факторы и т. д.), под внутренними — изменения у гомеотермных животных и человека, представляющие собой цегди сложнейших компенсаторных реакций в организме, возникших под влиянием изменений окружающей среды. Эти физиологические, биохимические, биофизические сдвиги порой настолько выражены (например, шок), что могут привести к гибели животных.
В большинстве случаев комбинация внешних и внутренних изменений приводит к нарушению как фармакокинетики (всасывания, времени циркуляции в крови, распределения по органам, биотрансформпции и элиминации лекарства), так и фармакодинамики, в связи с чем сила его действия может понижаться или повышаться в несколько раз.
Внешние условия оказывают влияние на реакцию лекарство — организм и основном с помощью не физико-химического, а физиологиче* скоро и биохимического механизмов.
Следует подчеркнуть, что о естественных условиях, как правило, наблюдаются многофакторные колебании внешних влияний. Например, при подъеме в горы, наряду с уменьшением содержания кислорода, повышается радиация, понижается барометрическое давление, изменяете» влажность воздуха и т. д. Ясно, что такие комплексные колебания условиям внешней среды отражаются на реакции организма к любым раздражителям, и том ЧНСЛС к лекарствам и ядам. При оценке значений того или иного компонента в действии лекарства нужно учитывать и то, ЧТО условно выделяемые нами факторы в свою очередь имеют сложный спектр, например воздух содержит С02, 02, N2, N02, CO К Т, д., соотношение И количество компонентов которых небезразлично для организма, И, наконец, следует учитывать интенсивность воздействии отдельных элементов внешней среды. До определенного уровня МОЖНО выделить специфическое влияние среды на фармакокинетику и фармакодинамику лекарств. С увеличением интенсивности в экстремальных условиях лекарство оказывает воздействие на фоне более менее выраженного стресса или шокового состояния.
Нервная система одна из первых реагирует на изменения окружающей среды, поэтому действие нейротропных веществ при изменении среды заметно моделируется. Одной из таких реакций является действие стимулятора центральной нервной системы фенамина на сгруппированных и одиночных (изолированных) животных. Острая токсичность препарата при внутрибрюшинном введении, по нашим данным, группе животных в 4 раза выше, чем у изолированных животных. А при чпероральном введении, когда в систему добавляется еще фактор всасывания в пищеварительном аппарате, токсичность фенамина для сгруппированных животных увеличивается в 11 раз. С другой стороны, длительная изоляция животного порождает у него агрессивность, и в таких условиях токсичность % же фенамина для мышей значительно повышается.
Резко влияет на действие лекарств температура окружающей среды. Различия могут быть не только количественными, но и качественными. Например, гидергин, эрготамин и серотонин вызывают у белых крыс гипертермию только при температуре выше 30 °С, при более низкой — гипотермию. Аминазин вызывает гипертермию при температуре выше 36 °С, 2,4-динитрофенол — выше 20 °С; при более низкой — снижается ректальная температура. Важно отметить, что при снижении температуры воздуха с 30 °С до 18°С токсичность аминазина для грызунов повышается почти в 3 раза.
Выраженные реакции возникают при введении атропина и других
холиноблокаторов. В связи с тем что холиноблокаторы нарушают пери
ферическую терморегуляцию путем угнетения потовых желез, введение
их в жаркое время может привести к фатальному исходу. У крыс
гидроксилирование ацетанилида микросомами печени при воздействии
холода повышается в 2 раза, у мышей метаболизм 2-нафтиламина при
воздействии холода ускоряется на 50%, при сочетанном действии
холода и шума — на 100 %.
Влияние температурного фактора на фармакодинамику лекарств необходимо учитывать в клинической практике, поскольку лекарства часто назначают при различных температурных режимах и больным с резко нарушенной терморегуляцией.
Однако даже эффекты лекарства одной фармакологической группы В условиях охлаждения могут быть противоположными. Так; гипотермия понижает нейромышечную блокаду, вызванную тубокурарином, и усиливает ее при введении дитилина.
Своеобразное влияние на действие лекарств оказывает лучевая энергия, После обнаружения фотодинамического эффекта акридина, то есть резкого возрастания отрицательного действия этого красителя на освещенных инфузорий, появилось много сообщений о роли различных видов лучистой энергии (гамма-лучей радиоактивных веществ, рентгеновских лучей, ультрафиолетовой видимой части спектра, инфракрасной радиации) в фармакодинамике лекарств. Установлено, что после курса рентгенотерапии у больных извращается действие кофеина. В первые часы после облучения снижается чувствительность животных к барбитуратам. На фоне лучевой терапии коразол утрачивает свое антидотное действие по отношению к барбитуратам.
Напротив, действие ионизирующей радиации и алкилирующих агентов, в частности противоопухолевых средств, потенцируется. Необходимо также помнить о том, что под влиянием ионизирующей радиации изменяются генетические, обменные процессы, что сопровождается нарушением кинетики ксенобиотика в организме.
Отмечено, что под влиянием ионизирующей радиации угнетается гидроксилирование стероидов, десульфурация глутатиона, образование парных соединений. Эти сдвиги могут быть причиной неожиданного извращенного действия лекарства на всех уровнях. В связи с этим при фармакотерапии больных, подвергшихся лучевой терапии, необходима большая осторожность.
Ультрафиолетовые лучи способствуют превращению холестерина в витамин D, который регулирует обмен кальция и фосфора в организме. Естественно, действие веществ, влияющих на минеральный обмен, при облучении ультрафиолетовыми лучами будет существенно изменяться. Существуют вещества, сенсибилизирующие организм к лучистой энергии. Кроме известных в настоящее время фотосенсибилизаторов (бероксан, аммифурин, псорален), следует назвать красители (эозин, трипафлавин, метиленовый синий и др.), нейротропные средства — барбитураты (барбитал, фенобарбитал) и производные фенотиазина (аминазин и др.), химиотерапевтические вещества (сульфамиды, в том числе и противодиабетические), антибиотики (тетрациклины), противогрибковые (гризеофульвин) и др. Конечно, механизм фотосенсибилизации очень сложен. В одних случаях под влиянием лучистой энергии образуются свободнорадикальные соединения, особенно соединения, содержащие -электронную систему, в других — под влиянием лекарства образуется порфирин, вызывающий фотосенсибилизацию; в третьих — возникает комплекс лекарства и белков, активизирующийся светом и трансформирующийся в антиген. На этом основании выделяют фототоксические и фотоаллергические реакции.
Более 100 лет тому назад было высказано предположение, что видимый свет выполняет не только оптическую, но и биологическую роль. Это становится понятным, если учесть, что между третьим нейроном сетчатки и вегетативными ядрами существуют ассоциативные связи. Принимая во внимание связи, существующие между этими ядрами и гипофизом, можно понять механизм влияния некоторых видов монохроматического света на шишковидную, щитовидную и половые железы. Сдвиги вегетативного фона и эндокринного профиля отражаются на колебаниях суточной эффективности лекарств. Известно, что строфантин, диуретические, снотворные, введенные вечером, действуют сильнее, чем в другое время суток. В литературе имеются данные об изменении токсичности в зависимости от биоритмов.
Очевидно, в процессе эволюции живых организмов выработались «биологический день» и «биологическая ночь»; этим можно объяснить многие сложные процессы действия лекарств при изменении освещенности .ШХ проявления биологической ритмики организма. В опытах па мышах установлено, что токсичность цитостатических средств (оли-помпцинп, 5-фторурацила) утром в 2 раза выше, чем вечером. Эти колебания токсичности хорошо коррелируют с периодичностью митотической активности клеток почек. Утром бетп-адрсноблокаторы действуют сильнее, чем введенные и ТАКОЙ же доля днем.
В последнее время привлекли к себе внимание проблема влияния на биологические процессы, втом числе на реакции органа на лекарства, магнитного поля. Установлено, что с возрастанием энергии магнитного поля и длительности его действия увеличивается реакция отдельных органов на медиаторы адреналин и ацетилхолин. В связи с тем что исследовании этом направлении только начались, можно ожидать новых интересных жданных об изменении действия лекарств под влиянием магнитного поля, которые будут использованы при создании рациональной фармакотерапии.
Современному человеку нужно осваивать космос и горные вершины, погружаться в мировой океан и подвергаться операциям в гипо- и гипербарических условиях. Поэтому крайне важно располагать данными об особенностях действия лекарств при различных видах гипоксии. Показано, что при гипобарической гипоксии повышается токсичность симпатомиметических аминов, увеличивается продолжительность сна в случае введения барбитуратов, усиливается депрессивное действие барбитала, хлоралгидрата, снимаются судороги после введения семикарбазида. В опытах на собаках установлено, что продолжительное пребывание в высокогорной местности усиливает гипотензивное действие папаверина и ослабляет — дибазола. Адаптация к высокогорным условиям сопровождается уменьшением разницы в действии лекарств по сравнению с контролем, но исходный уровень реактивности достигается редко,
Каждое химическое средство при гипоксии проявляет какие-то ему присущие свойства. Литературные данные, касающиеся действия лекарств на отдельные системы, органы, ткани, клетки, субклеточные структуры и ферменты дыхательной цепи при гипоксии, очень разноречивы. Можно ЛИШЬ отметить, что вещества, усиливающие обменные процессы, двигательную активность и возбуждающие нервную систему, отличаются повышенной токсичностью. В клинической практике приходится наблюдать различные виды гипоксии (гипоксическую, гемическую, циркуляторную и гистотоксическую), а еще чаще их ерчетанные формы. Рациональная фармакотерапия возможна только при учете особенностей действия лекарств.
К важным факторам формирования реакции организма на ксенобиотики относится характер питания. Известно, что лекарства быстрее всасываются натощак и медленнее — после еды. Голодание способствует угнетению биотрансформацни лекарств и, в частности, скорости гидроксилирования ацетаниламида, диметилирования меперидина, метаболизма гексобарбитала и других соединений, но не оказывает влияния на микросомальное восстановление паранитробензойной кислоты. У голодающих животных глюкуронидные парные соединения образуются в меньшем количестве, чем в норме, хотя активность ферментов при этом не снижается, ускоряется всасывание из пищеварительного аппарата лекарств, быстрее проявляется их токсическое действие. Общеизвестно, что во время голодания применение инсулина дает токсический эффект. В условиях белкового голодания, несмотря на введение в больших количествах витаминов, развиваются гипоавитаминозы в связи с нарушением синтеза белковой части ферментов, в состав которых н виде коэнэимов входят витамины.
Анализ литературных данных показывает, что изменение механизма действии лекарств на фоне различных гипо- и авитаминозов обусловлено специфическим компонентом, связанным с нарушением определенных звеньев метаболизма, и неспецифическим компонентом, связанным изменением реактивности организма.
В ряде случаев фармакологический эффект при углеводном питании существенно отличается от такового в контрольной группе. Количество случаев язвы желудка и эмбриотоксического эффекта под влиянием приема кислоты ацетилсалициловой у крыс, содержавшихся на углеводной пище, выше, чем у контрольных животных» получавших достаточном количестве белки.
Во взаимодействии ксенобиотиков с компонентами пищеварительного аппарата и пищи играет роль рН среды. Многие лекарства являются основаниями или кислотами, и в зависимости от степени ионизации существенно колеблется их всасывание и выделение из организма, что ФтраяяШтся и· их эффективности. С помощью пищевых продуктов растительного происхождения, содержащих в большом количестве калий, удпятен избежать побочного действия салуретиков, обусловленного гипокплиемией, Кроме того, прием пищи предотвращает раздражение некоторыми лекарствами слизистой оболочки пищеварительного аппарата при употреблении их внутрь (ПАСК, салицилаты, хлоралгидрат и др.).
Классический пример влияния компонентов пищи на действие ингибитором моноаминоксидазы. Если во время курса лечения ингибиторами моиоаминоксидаз употреблять сыр, бананы, фисташки, некоторые Вина и пиво» содержащие предшественники биогенных аминов (тира-мин, тирозин, триптофан), то вследствие нарушения дезаминирования последних может наступить гипертонический криз и даже кровоизлияние в мозг со смертельным исходом. Поэтому врачу необходимо очень тщательно анализировать характер и режим питания при назначении лекарств с целью оптимизации терапевтического эффекта.
К режиму питания примыкает водно-солевой режим. Известно» что водная нагрузка способствует увеличению диуреза потоотделения и Других видов секреции, а следовательно, элиминации ксенобиотиков из организма. Напротив, уменьшение введения жидкости способствует задержке выведения лекарств и их более продолжительному, подчас токсическому действию. Клиницисты хорошо знают и рационально попользуют эти закономерности при фармакотерапии и лечении отравлений. Наряду с водной нагрузкой в случае необходимости для регуляции терапевтического эффекта изменяют ионное равновесие. С целью усиления терапевтического эффекта бромидов назначают бессолевую Диету, а при появлении признаков бромизма вводят в большом количестве ионы хлора для ускорения выделения из организма ионов брома. Реализация действия лекарств в большой степени связана с кислотно-основным состоянием. Так, при метаболическом ацидозе понижается иалуретичеекий эффект ингибиторов карбоангидразы, но усиливается мочеотделение, стимулированное ртутными мочегонными.
Накопление экспериментального и клинического материалов позволит ив только прогнозировать величину терапевтического эффекта, но, что самое главное, на фоне конкретных условий внешней среды направленно его регулировать.
Конечно, кроме внешних факторов, существенное значение в интегральном ответе организма имеет исходное состояние организма. Можно выделить ряд функциональных особенностей и патологических состояний»
Из физиологических особенностей организма следует учитывать прежде всего массу тела. Ясно, что одна и та же доза лекарства у больных с массой тела 50 кг и 80 кг будет создавать соответственно разную концентрацию и давать различный эффект. Иногда прибегают также к определению роста, площади поверхности тела и других показателей, позволяющих подобрать оптимальную дозу лекарства.
Важное значение в фармакодинамике лекарств имеют возраст больного, половые различия. Известно, что многие фармакологические агенты дают извращенные реакции во время беременности (отхаркивающие — рвоту); при циклических состояниях у женщин (менструации) чаще повышается чувствительность к капилляроактивиым веществам (мышьяк, ртуть). Правда, не выявлено половых различий в скорости обезвреживания лекарств микросомальными ферментами печени. Все же, учитывая меньшую массу тела большинства женщин и повышенную чувствительность их к ряду лекарств, при назначении лекарств женщинам необходимо проявлять большую осторожность. Следует также учитывать эмбриотоксическое, тератогенное и мутагенное влияние многих лекарств.
Важную роль в фармакодинамике лекарств играет путь их введения, который выбирается врачом с учетом многих факторов. Максимальный эффект при минимальном латентном периоде наблюдается при подведении лекарств к местам действия (внутриартериально, внутривенно, внутрикардиально), и, наоборот, при пероральном введении те же дозы дают меньший эффект с большим латентным периодом.
Существенное значение имеет состояние организма. Так, прием
гипотензивных средств (ганглиоблокаторов) в терапевтических дозах
D лежачем положении хорошо переносится больными, а при вставании
может наступить ортостатический коллапс.
Фармакодинамика лекарств усложняется при различных патологических состояниях. Каждое заболевание как бы по-своему моделирует фармакологический эффект, в случае нескольких заболеваний картина еще более усложняется.
Конечно, при поражении печени преимущественно нарушается биотрансформация лекарств; болезни почек, как правило, сопровождаются
замедлением экскреции ксенобиотика. Однако такие однозначные фар-
макокинетические. модуляции наблюдаются редко, чаще фармакокине-
тические сдвиги переплетаются со сложными фармакодинамнческими
изменениями. Тогда не только при одном заболевании повышается или
понижается действие лекарства, но в течении заболевания отмечаются
существенные колебания, обусловленные как динамикой самого патологического процесса, так и применяемыми в процессе лечения средствами (индукция микросомальиых энзимов). Иногда при различных патологических состояниях действие лекарств изменяется в одном на
правлении, Так, больные с хроническими заболеваниями легких и с повышенным внутричерепным давлением очень чувствительны к морфину
и другим депрессантам дыхания. При гипертиреозе чувствительность
К морфину понижается, но резко повышается чувствительность к сим-
пштомиметическим аминам и т. д.
Следует иметь в виду, что некоторые лекарственные средства (жаропонижающие, противовоспалительные средства, сердечные гликомиды) в терапевтических дозах почти не действуют на здоровый организм и дают терапевтический эффект только при наличии патологии.
Для Спешного лечения заболеваний приходится одновременно или последовательно назначать несколько лекарственных средств, благодаря чему усиливается и удлиняется терапевтический эффект, снижаются токсические свойства или ликвидируется толерантность; возможны противоположные явления и даже непредвиденные реакции. Взаимодействие интегрируется либо на уровне фармакокинетических процессов (всасывание, распределение, превращение и выделение), либо в сочетании действия одного вещества с действием другого, т. е. в фармакодинамических реакциях. Эффективность и безвредность комбинированной терапии следует изучать точно так же, как изучают действие одного средства. Явление, возникающее при введении двух и более веществ, действующих в одном направлении, называется синергизмом. Его суммарный эффект может иметь два числовых значения: ![]() Если эффект равен сумме составляющих, говорят о суммировании действия, или аддитивном действии. Суммирование обнаруживается чаще при прямом синергизме, когда оба вещества действуют на одни и те же биологические структуры (адреналин и норадреналин). Явление, когда эта величина больше единицы
Если эффект равен сумме составляющих, говорят о суммировании действия, или аддитивном действии. Суммирование обнаруживается чаще при прямом синергизме, когда оба вещества действуют на одни и те же биологические структуры (адреналин и норадреналин). Явление, когда эта величина больше единицы ![]() , называется потенцированием (супрааддитивное, или инфрааддитивное, действие); обычно это характерно для косвенного синергизма, когда два и больше веществ действуют на разные образования (ацетилхолин и прозерин). Кроме того, выделяют еще два вида комбинированного действия — гетергическое, когда из двух веществ лишь одно дает изучаемый эффект, а в спектре второго вещества такого вида действие не определяется, и гомергическое, когда оба вещества проявляют одинаковое действие в отдельности.
, называется потенцированием (супрааддитивное, или инфрааддитивное, действие); обычно это характерно для косвенного синергизма, когда два и больше веществ действуют на разные образования (ацетилхолин и прозерин). Кроме того, выделяют еще два вида комбинированного действия — гетергическое, когда из двух веществ лишь одно дает изучаемый эффект, а в спектре второго вещества такого вида действие не определяется, и гомергическое, когда оба вещества проявляют одинаковое действие в отдельности.
Явление, характеризующееся ослаблением фармакологического эффекта одного вещества при введении другого ![]() , называется антагонизмом. Его широко используют на практике для лечения отравлений и коррекции отрицательного действия лекарств (налоксон при лечении отравлений и для устранения депрессии дыхания морфином). В зависимости от первичных реакций различают физический, химический
, называется антагонизмом. Его широко используют на практике для лечения отравлений и коррекции отрицательного действия лекарств (налоксон при лечении отравлений и для устранения депрессии дыхания морфином). В зависимости от первичных реакций различают физический, химический ![]()
![]() и физиологический, или функциональный, антагонизм. В основе функционального антагонизма лежат более сложные процессы, поэтому в зависимости от биохимического субстрата, с которым взаимодействуют антагонисты; выделяют такие виды антагонизма: 1) конкурентный, 2) неконкурентный, 3) бесконкурентный, 4) независимый, 5) неравновесный. В основном врачу приходится иметь дело с двумя видами антагонизма — конкурентным (два вещества взаимодействуют с одними и теми же рецепторами) и неконкурентным (антагонисты реагируют с разными структурами, участвующими м каскадном процессе эффекта).
и физиологический, или функциональный, антагонизм. В основе функционального антагонизма лежат более сложные процессы, поэтому в зависимости от биохимического субстрата, с которым взаимодействуют антагонисты; выделяют такие виды антагонизма: 1) конкурентный, 2) неконкурентный, 3) бесконкурентный, 4) независимый, 5) неравновесный. В основном врачу приходится иметь дело с двумя видами антагонизма — конкурентным (два вещества взаимодействуют с одними и теми же рецепторами) и неконкурентным (антагонисты реагируют с разными структурами, участвующими м каскадном процессе эффекта).
Кроме того, известны случаи, когда одно вещество действует па различные рецепторы, индуцирующие противоположные силы в одном фармакологическом эффекте, это явление называют аутоантагонизмом. Он проявляется при изменении концентрации вещества и может быть бесконкурентным, неконкурентным и независимым.
Кроме синергизма и антагонизма, существуют такие понятия, как синерго-антагонизм или антагонизмо-синергизм, когда два вещества в зависимости от дозы проявляют явления и синергизма, и антагонизма.
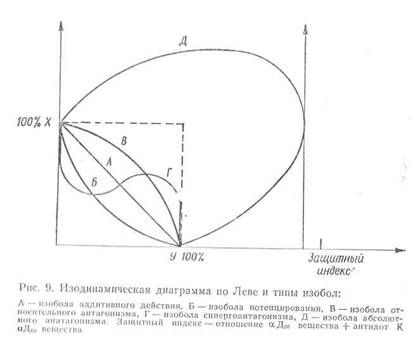
И, наконец, возможны такие ситуации, когда два и больше веществ дают совершенно новый, так называемый парадоксальный эффект, не присущий ни одному из взятых в отдельности веществ. Все возможные варианты комбинированного действия представлены на рис. 9.
Следует подчеркнуть, что результаты комбинированного действия могут рассматриваться лишь относительно определенного эффекта и соответствующих доз; относительно других эффектов и доз могут быть получены прямо противоположные данные. Таким образом, знание фармакодинамики лекарства позволяет врачу управлять лечебным процессом и индивидуализировать фармакотерапию.
Использованная литература
1. Справочник по клинической фармакологии и фармакотерапии Чекман И.С, Пелещук А.П., Пятак О.А. и др.; Под ред. И.С. Чекмана, А.П. Пелещука, О.А. Пятака.— К. : Здоровя, 1987...—736 с.