Соединения, изолируемые перегонкой с водяным паром: кетоны - ацетон
СОДЕРЖАНИЕ: Свойства и практическое применение ацетона. Оценка уровня токсичности данного вещества, распространение отравлений. Биотрансформация, токсикокинетика ацетона, клиника отравления, диагностика, детоксикация. Проведение химико-токсикологического анализа.Реферат
Соединения, изолируемые перегонкой с водяным паром: кетоны: ацетон
1. Свойства и применение ацетона
Ацетон

Синонимы: Диметилкетон, 2-пропанон
1.1 Свойства
Ацетон – это бесцветная горючая жидкость с характерным запахом. Смешивается со спиртом, эфиром и водой в любых соотношениях. Не образует азеотропной смеси с водой. Из водных растворов ацетон высаливается хлоридом натрия, хлоридом кальция, карбонатом калия (жидкость разделяется на два слоя). Ацетон хорошо растворяет соли многих неорганических кислот и ряд органических соединений. Ацетон получают при сухой перегонке дерева, каменного угля, а также путем синтеза. 3-й класс опасности, хорошо смешивается с водой и спиртом, смесь ацетона и воздуха взрывоопасна.
Таблица 1.1 Свойства ацетона
| Молекулярный вес | 58,08 |
| Температура плавления | -95,35 0 С |
| Температура кипения | 56,24 0 С |
| Температура вспышки | -18 °С |
| Температура самовоспламенения | 500 °С |
| Температурные пределы воспламенения паров в воздухе | нижний – -20 °С верхний – 6 °С |
| Концентрационные пределы воспламенения паров в воздухе | нижний – 2,2% (по объему) верхний – 13% (по объему) |
| Минимальная энергия зажигания паров в воздухе | 0,6 мДж |
| Плотность | 0,79 г./см3 |
| Дипольный момент при 2 Дебай | 2,72 |
| Вязкость, сантипуазы при 15 С | -0,3371 |
| Поверхностное натяжениепри 20 С | : 23,32 дины на сантиметр |
| Показатель преломления | 1,358825 |
Ацетон обладает всеми химическими св-вами, характерными для алифатических кетонов. Он образует кристаллические соединения с гидросульфитами щелочных металлов, например с гидросульфитом натрия – (CH3 )2 C(OH) SO3 Na.
Только сильные окислители, например щелочной раствор калия перманганата и хромовая кислота, окисляют ацетон до уксусной и муравьиной кислот и далее – до СО2 и воды.
Каталитически ацетон восстанавливается до изопропанола, амальгамамы Mg или Zn, а также цинком с уксусной кислотой – до пинакона.
Атомы водорода в ацетоне легко замещаются при галогенировании, нитрозировании и т.п. Действием хлора и щелочи (напр. натрия гидроксидом) ацетон превращается в хлороформ, который взаимодействует с ацетоном с образованием хлорэтона, применяемого как антисептик.
Ацетон окисляет вторичные спирты в присут. алкоголятов Аl до кетонов.
Ацетон вступает в альдольную конденсацию с образованием диацетонового спирта, а также в кротоновую конденсацию с образованием окиси мезитила (СН3 )2 С=СНСОСН3 , форона (СН3 )2 С=-СНСОСН=С(СН3 )2 и мезитиленацетона.
В присутствии сильной минеральной кислоты (например серная кислота) ацетон алкилирует фенол с образованием дифенилолпропана (бисфенола ацетона) (НОС6 Н4 )2 С(СН3)2 , присоединяет цианид- ион с образованием ацетонциангидрина (CH3)2 C(OH) CN.
При пиролизе (700 °С) ацетона образуются кетен СН2 =С=О и метан.
1.2 Применение
В промышленности ацетон получают преимущественно так называемым кумольным способом одновременно с фенолом из бензола и пропилена через изопропилбензол (кумол) по схеме:
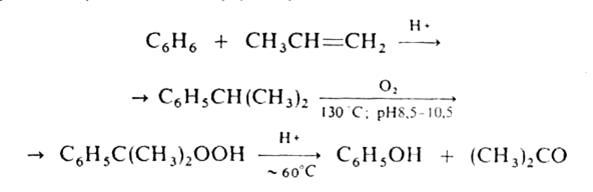
В ряде других промышленных способов синтеза ацетон исходят из изопропанола:
1. Окисление в паровой фазе (катализатор – металлический Cu, Ag, Ni или Pt):
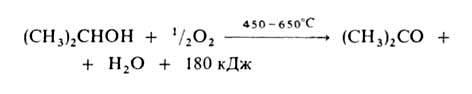
Высокий выход ацетона (90%) достигается при использовании Ag, осажденного на пемзе, или серебряной сетке.
2. Автокаталитическое окисление в жидкой фазе при 90–140 °С и 0,2–0,3 МПа:
![]()
Выход ацетона 95% от теоретического, Н2 О2 87%.
3. Дегидрирование в паровой фазе в присутствии ZnO, осажденной на пемзе:
![]()
Степень превращения изопропанола в ацетон при 225 °С составляет 84% при 380 °С – 98%, при 525 °С – 100%. Выход ацетона около 90%.
Новый промышленный способ получения ацетона – прямое окисление пропилена в жидкой фазе в присутствии PdCl2 в среде водного раствора солей Pd, Fe или Cu при 50–120 °С и 5–10 МПа:

Выход ацетона 90%. Некоторое значение сохранил способ получения ацетона брожением крахмала под влиянием бактерий Bacyllus acetobutylicus, превращающих крахмал в ацетон и бутанол (так называемое ацетоновое брожение). Известны и др. способы получения:
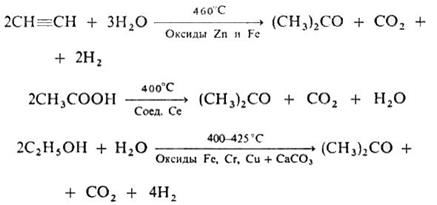
Технический ацетон широко применяется в лакокрасочной промышленности в качестве растворителя нитролаков, нитроэмалей (при выработке авиационных, автомобильных, кабельных, кожевенных и других лаков), при получении ацетилцеллюлозы и нитроцеллюлозы, в производстве некоторых сортов искусственного шёлка, при изготовлении органического небьющегося стекла, в производстве киноплёнок, бездымного пороха, целлулоида, акрихина и других.
Способность ацетона растворять ацетилен используется в широких масштабах при наполнении стальных баллонов, в которых хранится ацетилен, применяемый для сварки металлов. Ацетилен поглощается пористым материалом, пропитанным ацетоном; при давлении 15 атм. 1 объём он растворяет 375 объёмов ацетилена.
Применение ацетона для извлечения воска из смазочных масел приобретает всё большее значение. Ацетон служит сырьём для производства многих химических продуктов: синтетического каучука, индиго, ионона (духи), сульфонала (снотворное средство). Соединения ацетона с солями сернистой и гидросернистой кислот применяют при крашении и печатании тканей.
Технический ацетон находит применение в производстве искусственной кожи, для обеззараживания шерсти и меха, для извлечения эфирных масел. Чистый ацетон применяется в пищевой промышленности при экстрагировании пищевых продуктов, витаминов, жиров; для экстрагирования некоторых лекарств и приготовления фармацевтических препаратов, требующих химически чистого растворителя с низкой температурой кипения.
Также его применяют для обезжиривания поверхностей или изделий используемых в промышленности и в быту.
Ацетон широко используется в промышленности как растворитель для извлечения ряда веществ, для перекристаллизации химических соединений, химической чистки, получения хлороформа и т.д. Пары ацетона тяжелее воздуха. Поэтому в помещениях, в которых происходит испарение ацетона, создается опасность отравления при вдыхании его паров.
2. Токсичность ацетона и распространенность отравлений
2.1 Токсичность ацетона
Ацетон сравнительно мало токсичен. Нелсон и др. нашли, что максимально допустимая концентрация ацетона в воздухе при 8-часовом воздействии составляет 0,02%. Дринкер и Кук считают, что максимально допустимая концентрация ацетона равна 0,05–0,25%. Смит и Майерс приводят случаи острого отравления парами смеси ацетона и бутанона при концентрациях порядка 0,1%. Неопубликованные исследования Штернера, Оглезби и Фассета показали, что из всех растворителей, применяемых в промышленности, ацетон является одним из наименее токсичных и в этом отношении вполне сравним с этиловым спиртом. В настоящее время максимально допустимой концентрацией принято считать 0,1%. Пребывание в течение короткого времени в атмосфере, в которой концентрация ацетона намного превышает указанную, не причиняет вреда.
Пределы воспламенения в воздухе 2,55–12,8 об.%.
Ацетон является естественным метаболитом организма человека и животных. Он входит в триаду соединений (бета-оксибутират, ацетоацетат и ацетон), обозначаемых, как кетоновые тела. Ацетон образуется путем неферментативного декарбоксилирования ацетоуксусной кислоты.
В нормальных условиях содержание ацетона в сыворотке крови человека обычно не превышает 6 мг/л (0,1 ммоль/л). Трехдневное голодание приводит к увеличению концентрации ацетона в сыворотке у лиц с ожирением до 17 мг/л, а у здоровых людей, не страдающих ожирением до 44 мг/л
В условиях дефицита глюкозы (голодание) или при снижении ее биодоступности (сахарный диабет), содержание кетоновых тел в крови может возрастать в десятки раз. При этом они действуют и как часть регуляторного механизма с обратной связью, блокируя чрезмерную мобилизацию жирных кислот из жировой ткани и ослабляя тем самым токсическое действие последних.
Токсичность ацетона, поступающего в организм извне хорошо изучена. Острая токсичность ацетона (LD50), поступающего через желудок составляет по данным разных авторов для крыс – 5,8–9,8 г/кг, для мышей – 3,0–5,25 г./кг, для кроликов и собак – 3,8–8,0 г/кг. По этому показателю ацетон мало отличается от этанола.
Эффективная однократная действующая доза (EDmin) ацетона для человека, определяемая по его влиянию на нервную систему, почки и кровь при условии поступления через желудок, составляет 2,9 г/кг.
Доза, обладающая минимальным токсическим действием (ПДхр.), определяемая на крысах при условии внутрижелудочного введения ацетона на протяжении 6 мес. составляет 7 мг/кг.
Его предельно допустимая концентрация (ПДК) в воде общего пользования составляет 2,2 мг/л.
Токсическое действие ацетона связано с наркотическим влиянием на ЦНС, прижигающим действием на слизистую оболочку дыхательных путей и органов пищеварения, метаболическим ацидозом и негативным влиянием на развитие плода.
Смертельная доза для человека – более 100 мл.
Токсическая концентрация в крови 200 – 300 мг/л, смертельная – 550 мг/л.
2.2 Распространенность отравлений
Благодаря широкому применению ацетона создается потенциальная возможность отравлений им, однако для действия ацетона нужны очень высокие концентрации его в крови; накопление же ацетона протекает крайне медленно, поэтому внезапных острых отравлений ацетоном путем вдыхания не происходит, хотя он и обладает токсическим действием.
Обычно острое отравление жидким ацетоном возникает, когда ацетон и жидкости, содержащие его, хранятся небрежно, в жилом помещении, тем более вблизи от продуктов и в посуде из-под напитков.
Случайные отравления гораздо чаще происходят в домашних условиях, чем на производстве, и обычно бывают острыми; промышленные отравления более часто являются результатом хронического воздействия. Случайное отравление происходит чаще всего в результате проглатывания токсичных веществ, чаще всего от этого страдают дети. В 15% случаев отравляющими веществами являются химические вещества, которые используются в быту, к которым и относится ацетон.
Вдыхание паров ацетона используется токсикоманами для достижения эйфории, поэтому часто пострадавшими являются подростки. Также встречаются и суицидальные отравления ацетоном.
3. Биотрансформация, токсикокинетика ацетона, клиника отравления, клиническая диагностика, методы детоксикации.
3.1 Биотрансформация и токсикокинетика ацетона
По фармакологическим свойствам ацетон относится к числу веществ, проявляющих наркотическое действие. Он может поступать в организм с вдыхаемым воздухом, а также через пищевой канал и кожу. После поступления ацетона в кровь часть его переходит в головной мозг, селезенку, печень, поджелудочную железу, почки, легкие и сердце. Содержание ацетона в указанных органах несколько меньшее, чем в крови. Он обладает кумулятивными свойствами. Ацетон медленно выводится из организма.
Незначительная часть ацетона, поступившего в организм, превращается в оксид углерода (IV), который выделяется с выдыхаемым воздухом. Некоторое количество ацетона выделяется из организма в неизменном виде с выдыхаемым воздухом и через кожу, а некоторое – с мочой.
В малых количествах ацетон может содержаться в норме в моче человека, а при глубоком расстройстве обмена веществ концентрация его в моче значительно возрастает. Нормальным содержанием ацетона в крови является 0,7–0,8 мг%. В суточном объеме мочи может содержаться 20–30 мг ацетона. У больных диабетом следы ацетона можно обнаружить во выдыхаемом воздухе.
3.2 Клиника отравления
Клиническая картина сходна с алкогольной интоксикацией. Однако коматозное состояние не достигает большой глубины.
При употреблении через рот смертельная доза составляет 60–70 мл и выше. Отмечается выраженное воздействие на центральную нервную систему. Появляются тошнота, рвота, боли в животе, цианоз кожи, при значительном количестве принятого ацетона человек достаточно быстро теряет сознание. Смерть может наступить уже через 6–12 часов после употребления ацетона.
Слизистая оболочка полости рта и глотки отечна, воспалена. Изо рта – запах ацетона. Часто возникают токсические гепато- и нефропатия, реактивный панкреатит, наблюдаются увеличение и болезненность печени, желтушность склер. Возможно появление признаков острой почечной недостаточности (снижение диуреза, появление белка и эритроцитов в моче). Часто развиваются бронхит и пневмонии.
При отравлении парами ацетона отмечается слабый наркотический эффект – головокружение, головная боль, шаткая походка, общая слабость, а также симптомы раздражения слизистых оболочек, конъюнктивит, ринит, стомаэзофагит, гастрит. При поступлении большой дозы ацетона ввиваются нарушения сознания вплоть до коматозного состояния глубокое шумное дыхание, метаболический ацидоз, шок. При высокой концентрации ацетона в воздухе, особенно в закрытых помещениях, возможно быстрое наступление летального исхода вследствие рефлекторной остановки дыхания.
Тяжелое ингаляционное отравление характеризуется расстройством зрения, судорогами, повышением концентрации сахара в крови, в дальнейшем потерей сознания. На вскрытии обнаруживается полнокровие внутренних органов, темная кровь в сердце и сосудах, запах ацетона от внутренних органов.
3.3 Клиническая диагностика
Клиническая диагностика основана на данных:
1. осмотра места происшествия (обнаруживают вещественные доказательства отравления – посуду из-под алкогольных напитков или суррогатов, упаковку от домашних химикатов или лекарств, запах химических веществ, характер рвотных масс и др.);
2. анамнеза (со слов пострадавшего или окружающих выясняют вид или название токсического вещества, принятого пострадавшим, время приема токсического вещества, дозу принятого токсического вещества, пути поступления яда в организм, обстоятельства, сопутствующие развитию отравления, и полученные сведения фиксируют в направительном документе);
3. изучения клинической картины заболевания для выделения специфических симптомов отравления, характерных для воздействия на организм определенного вещества или группы веществ по принципу так называемой избирательной токсичности. На догоспитальном этапе чрезвычайно важно зарегистрировать основные клинические симптомы и их изменение под влиянием специфической (антидотной) и иной терапии.
Лабораторная токсикологическая диагностика направлена на качественное или количественное определение (идентификацию) токсических веществ в биологических средах организма (крови, моче и пр.).
Тест-полоски» Кетофан для анализа ацетона в моче (Keto Phan, кетоновые тела).
Тест полоски для анализа уровня кетоновых тел в моче (ацетона). Тест основан на реакции Легала. Цветная шкала сравнения на этикетке отражает концентрацию ацетоуксусной кислоты в моче.
Диапазон показаний: отриц., 1.5, 3, 7.5, 15 м/моль ммоль/л
Время измерения: 60 с
Условия хранения: Диагностические полоски должны храниться в плотно закрытой заводской таре в сухом и темном месте (с +2 до +30) градусов
Реагент Легала. 1%-ный раствор нитропруссида в 50%-ном этанольном растворе 1 М NaOH.
Ацетон с нитропруссидом натрия в щелочной среде дает интенсивно-красную окраску. При подкислении уксусной кислотой окраска переходит в красно-фиолетовую:
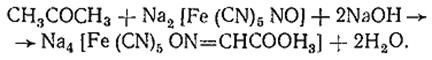
С нитропруссидом натрия окрашенные соединения образуют вещества, содержащие енолизируемые СО-группы
![]()
Кетоны, в молекулах которых отсутствуют метильные или метиленовые группы, связанные с СО-группами, не дают этой реакции.
3.4 Методы детоксикации
Детоксикация – это процесс обезвреживания ядов и ускорения их выделения из организма. Различные методы детоксика-ции способствуют освобождению желудка и кишок от еще невсо-савшегося в кровь яда, а также освобождению крови и тканей организма от находящихся в них токсического вещества и его метаболитов.
Лечение зависит от пути поступления яда. Оно должно быть направлено на уменьшение адсорбции токсического вещества (промывание желудка с помощью зонда или кожных покровов, обеспечение доступа свежего воздуха и т.д.).
Обязательно проводят инфузионную терапию изотоническими и кристаллоидными растворами (для профилактики и лечения экзотоксического шока). Введение ощелачивающих растворов (натрия гидрокарбоната, трисамина, «Лактасола») позволяет устранить метаболический ацидоз. (Применение антидотов является эффективным способом детоксикации только на ранней стадии острых отравлений.)
Рекомендуются форсированный диурез – больным внутривенно вводят 1,5–2 л жидкости (изотонический раствор хлорида натрия, 5%-й раствор глюкозы и др.)· Для стимуляции диуреза назначают диуретические средства. Ими могут быть так называемые осмотические диуретики (15–20%-е растворы мочевины или маннита). После внутривенного вливания раствора диуретика вводят растворы электролитов, содержащих ионы калия и натрия, со скоростью, равной скорости диуреза (500–800 мл/ч).
При тяжелых отравлениях ацетоном применяют гемодиализ и гемосорбцию.
· Гемосорбция (гемоперфузия) является одним из способов искусственной детоксикации организма. Этот метод основан на поглощении сорбентами ядовитых веществ, находящихся в крови. При гемосорбции в качестве сорбентов в основном применяются активированный уголь и ионообменники (иониты). Гемосорбцию проводят с помощью прибора (детоксикатора), снабженного насосом для перекачивания крови и набором колонок (капсул), содержащих указанные выше сорбенты. Этот аппарат с помощью специального приспособления подключают к кровотоку больного. Кровь, проходящая через сорбенты, освобождается от токсических веществ, которые поглощаются этими сорбентами.
· Гемодиализ – один из эффективных методов ускорения выведения токсических веществ из организма. Он основан на явлении диализа, используемого для освобождения крови от токсических веществ. Гемодиализ проводится с помощью аппарата, известного под названием «искусственная почка». Этот аппарат снабжен полупроницаемой мембраной, через которую из крови переходят токсические вещества в процессе гемодиализа.
4. Объекты исследования. Особенности подготовки проб и изолирования
Внутренние органы трупа редко являются объектами химико-токсикологического анализа. Гораздо чаще в качестве объектов встречаются кровь, моча и выдыхаемый воздух.
Кровь отбирается из поверхностной вены через иглу самотеком в сухой пенициллиновый флакон, содержащий раствор гепарина (3–5 капель на каждые 10 мл крови). Флакон закрывается стандартной резиновой пробкой, которую фиксируют алюминиевым колпачком. Содержимое флакона сразу же перемешивают. Для химико-токсикологического исследования необходимо не менее 10 мл крови.
Моча отбирается в чистый сухой флакон в количестве не менее 10 мл. Флакон закрывается стандартной резиновой пробкой, которую фиксируют алюминиевым колпачком.
Органы трупа, предварительно тщательно измельчают (при помощи ножниц, придерживая объект пинцетом), смешивают с дистиллированной водой до густоты кашицы и помещают в круглодонную колбу, заполняя последнюю не более чем на 1/3 ее объема.
Изолирование ацетона проводят методом дистилляции с водяным паром.
Дистилляция с водяным паром производится в специальном приборе (рис. 4.1)
Исследуемый объект помещают в круглодонную колбу, заполняя последнюю не более чем на 1/3 ее объема. Колбу (2) с объектом исследования закрепляют в штативе и погружают в холодную водяную баню (3). Затем все части прибора соединяют встык. Объект исследования быстро подкисляют до рН 2 – 2,5, немедленно соединяют с заранее нагретым парообразователем (1) и нагревают до кипения водяную баню и парообразователь. Для подкисления используют щавелевую или виннокаменную кислоту.
Пропускание пара вместо образования его в самой колбе с объектом исследования важно потому, что при пропускании пара колбу с объектом можно нагревать (чтобы не конденсировались пары) на водяной бане. Образование пара в колбе потребовало бы нагревания при температуре выше 100° на пламени или масляной бане и могло бы повести к разложению веществ на стенках колбы выше уровня воды и даже к образованию следов синильной кислоты за счет подгорания белковых веществ.
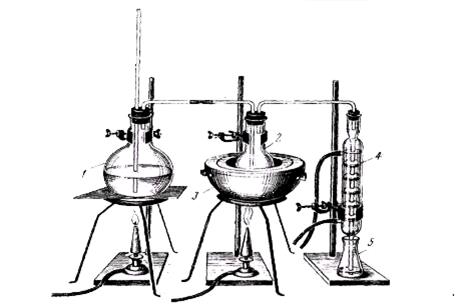
Рис. 4.1. Прибор для дистилляции с водяным паром.
1 – парообразователь; 2 – колба с объектом исследования; 3 – баня водяная; 4 – холодильник шариковый; 5 – приемник дистиллята.
Дистилляция должна проводиться по возможности медленно, что достигается регулированием пламени горелок. Первый дистиллят, сконденсированный в холодильнике (4), собирают в объеме 3 мл в заранее приготовленную коническую колбу (5), содержащую 2 мл 2% раствора едкого натра; остальные дистилляты по 25–50 мл собирают в последующие 1–2 колбы, также подготовленные заранее. Для качественного исследования продукта перегонки с водяным паром в большинстве случаев бывает достаточно собрать 25 мл второго дистиллята.
При положительных результатах реакций на то или иное вещество, имеющее токсикологическое значение, дистилляцию продолжают до тех пор, пока дистиллят не перестанет давать соответствующих качественных реакций. Дистилляты подвергают качественному исследованию, а при положительных результатах анализа в них определяют количества найденных веществ.
5. Методы качественного и количественного химико-токсикологического анализа (ХТА)
В химико-токсикологическом анализе для обнаружения ацетона применяют реакции с растворами иода, нитропруссида натрия, фурфурола, о – нитробензальдегида и метод микродиффузии.
1. Реакция образования йодоформа. При взаимодействии ацетона с раствором иода в щелочной среде образуется йодоформ:

Выполнение реакции. К 1 мл исследуемого раствора прибавляют 1 мл 10%-го раствора аммиака и несколько капель раствора иода в иодиде калия. В присутствии ацетона образуется желтый осадок йодоформа с характерным запахом, а его кристаллы имеют характерную форму.
Предел обнаружения: 0,1 мг ацетона в пробе.
Эту реакцию дает и этиловый спирт.
2. Реакция с нитропруссидом натрия. Ацетон с нитропруссидом натрия в щелочной среде дает интенсивно-красную окраску. При подкислении уксусной кислотой окраска переходит в красно-фиолетовую:

С нитропруссидом натрия окрашенные соединения образуют вещества, содержащие енолизируемые СО-группы
![]()
Кетоны, в молекулах которых отсутствуют метильные или метиленовые группы, связанные с СО-группами, не дают этой реакции.
Выполнение реакции. К 1 мл исследуемого раствора прибавляют 1 мл 10%-го раствора гидроксида натрия и 5 капель 1%-го свежеприготовленного раствора нитропруссида натрия. При наличии ацетона в пробе появляется красная или оранжево-красная окраска. При добавлении 10%-го раствора уксусной кислоты до кислой реакции через несколько минут окраска переходит в красно-фиолетовую или вишнево-красную.
Такую же окраску с нитропруссидом натрия дает метилэтилкетон. Другие окраски с этим реактивом дают ацетофенон, ацетилацетон, ацетоуксусный эфир, диацетил, коричный альдегид и др.
3. Реакция с фурфуролом. Эта реакция основывается на способности ацетона конденсироваться с фурфуролом и некоторыми другими альдегидами (ванилин, салициловый альдегид) с образованием окрашенных соединений:

Выполнение реакции. К 1 мл исследуемого раствора прибавляют 5 капель 1%-го раствора фурфурола в этиловом спирте (96°) и 3 капли 10%-го раствора гидроксида натрия. Через 3– 5 мин к этой жидкости прибавляют 10–12 капель концентрированной соляной кислоты. При наличии ацетона появляется красная окраска.
Эта реакция не специфична для обнаружения ацетона. Ее дают некоторые альдегиды и кетоны.
4. Реакция с о – нитробензальдегидом. При взаимодействии ацетона с о-нитробензальдегидом в щелочной среде образуется индиго, имеющее синюю окраску:
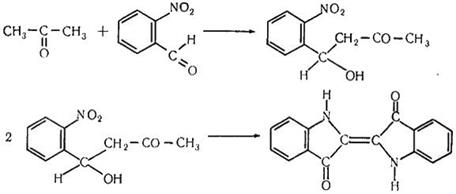
Малые количества ацетона с о – нитробензальдегидом реагируют медленно. При этом сначала появляется желтая окраска, переходящая в желто-зеленую, а затем в зелено-синюю. Образовавшееся при этой реакции индиго хорошо экстрагируется хлороформом, который приобретает синюю окраску.
Выполнение реакции. В пробирку вносят 3–5 капель исследуемого раствора и каплю насыщенного раствора о-нитробенз-альдегида в 2 н. растворе гидроксида натрия. Смесь слегка нагревают на водяной бане, а затем охлаждают до комнатной температуры. После этого в пробирку прибавляют 1 мл хлороформа и взбалтывают. При наличии ацетона хлороформный слой приобретает синюю окраску.
Предел обнаружения: 100 мкг ацетона в пробе.
При указанных выше условиях спиртовые растворы ацетона дают сине-красную окраску. о – Нитробензальдегид также дает окраску с ацетофеноном, ацетилацетоном, диацетилом, ацетоуксусным эфиром, ацетальдегидом и др.
5. Метод микродиффузии широко используется в биохимических и некоторых токсикологических лабораториях для обнаружения химических соединений, имеющих большую упругость паров.
Для обнаружения исследуемых веществ методом микродиффузии применяют чашки Конвея или подобные им сосуды, в которых летучие вещества из исследуемых объектов сначала переходят в пространство прибора, а затем в соответствующий растворитель или в раствор реактивов, реагирующих с определяемыми веществами.
Метод микродиффузии имеет ряд достоинств. Он позволяет обнаружить летучие вещества, содержащиеся в небольших количествах исследуемых объектов. При использовании этого метода не образуется пена (что возможно при перегонке летучих ядовитых веществ с водяным паром), определяемые вещества не подвергаются сильному разбавлению и т.д.
Скорость диффузии зависит от упругости пара исследуемого вещества, объема пробы, температуры, состава поглощающих жидкостей и т.д. На скорость перехода отдельных летучих веществ из исследуемых объектов в пространство прибора для микродиффузии влияют некоторые электролиты. Так, например, прибавление насыщенного раствора карбоната калия к крови, моче и гомогенатам тканей, содержащих этиловый спирт, ускоряет переход этого спирта в пространство прибора. Для ускорения перехода других соединений из исследуемых объектов в пространство прибора прибавляют кислоты, щелочи и др.
Прибор для микродиффузии (рис. 1) представляет собой небольшой круглый толстостенный сосуд 1 из стекла или пластмассы (наружный диаметр 60–70 мм, высота 10 мм). Внутри этого сосуда расположен второй круглый сосуд 2 меньшего размера (диаметр 30–35 мм, высота 5 мм). Таким образом, в приборе для микродиффузии имеется внутренняя круговая 3 и наружная кольцевая 4 камеры. Верхний край наружной камеры должен пришлифовываться так, чтобы к нему плотно прилегала крышка 5.

Рис. 5.1 Прибор для микродиффузии
Для создания герметичности в приборе края наружной камеры слегка смазывают вазелином или силиконовой смазкой и плотно прижимают крышку.
Исследуемые объекты вносят в наружную кольцевую камеру, а поглощающую жидкость – во внутреннюю камеру. К. исследуемым объектам, находящимся в наружной камере прибора, на расстоянии 2–3 см помещают раствор вещества, способствующего переходу исследуемого соединения из объекта в пространство прибора. Затем прибор плотно закрывают крышкой и слегка наклоняют его для смешивания исследуемого объекта и раствора, способствующего переходу исследуемого вещества в пространство прибора. После этого прибор оставляют на определенное время, необходимое для диффузии. После окончания диффузии определяют исследуемое вещество в жидкости, находящейся во внутренней камере.
Обнаружение ацетона. В наружную камеру прибора для микродиффузии вносят 3 мл крови или мочи, или 1 г гомогената тканей. Затем в ту же камеру вносят 3–4 капли 10%-го раствора серной кислоты. Во внутреннюю камеру прибора вносят 3,3 мл 0,15 раствора гидросульфита или сульфита натрия. Прибор плотно закрывают крышкой и оставляют на 4 ч при комнатной температуре.
После окончания микродиффузии из внутренней камеры прибора берут 1 мл жидкости и переносят ее в пробирку, в которую прибавляют 9 мл воды, 4 мл 40%-го раствора гидроксида натрия, 1 мл 20%-го свежеприготовленного раствора салицилового альдегида в этиловом спирте. Пробирку в течение трех минут нагревают на водяной бане (при 50–60 °С), а затем охлаждают до комнатной температуры. При наличии ацетона в пробе появляется красная окраска.
Количественное определение ацетона основано на образовании йодоформа при взаимодействии его со щелочным раствором: йода. Избыток йода после подкисдения оттитровывают 0,1 н. раствором тиосульфата натрия, индикатор – раствор крахмала.
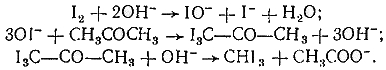
I2 + Na2 S2 O3 Na I + Na2 S2 O4
6. Оценка результатов исследования
Являясь хорошим растворителем нитроклетчатки, ацетилклетчатки и смол, ацетон в больших количествах используется при производстве бездымного пороха, искусственного шелка и т.д.; он является исходным материалом для получения каучука и некоторых лекарственных веществ. Благодаря широкому применению ацетона создается потенциальная возможность отравлений им, однако для действия ацетона нужны очень высокие концентрации его в крови; накопление же ацетона протекает крайне медленно.
Токсическое действие ацетона связано с наркотическим влиянием на ЦНС, прижигающим действием на слизистую оболочку дыхательных путей и органов пищеварения, метаболическим ацидозом и негативным влиянием на развитие плода.
Смертельная доза для человека – более 100 мл.
Токсическая концентрация в крови 200 – 300 мг/л, смертельная – 550 мг/л.
В малых количествах ацетон может содержаться в норме в моче человека, а при глубоком расстройстве обмена веществ концентрация его в моче значительно возрастает. Нормальным содержанием ацетона в крови является 0,7–0,8 мг%. В суточном объеме мочи может содержаться 20–30 мг ацетона.
Список используемой литературы
1. Ацетон технический, ГОСТ 2768–84;
2. МЗ РФ ПРИКАЗ от 5 октября 1998 г. №289 «Об аналитической диагностике наркотических средств, психотропных и других токсических веществ в организме человека»;
3. Кружалов Б.Д., Голованенко Б.И., Совместное получение фенола и ацетона, М, 1963;
4. Теддер Дж., Нехватал А., Джубб А., Промышленная органическая химия, пер. с англ., М., 1977;
5. Токсикологическая химия: учебник для вузов/ под ред. Плетеневой. – 2-е изд., испр. – М.: ГЭОТАР-Медиа, 2006. – 512 с.;
6. Швайкова М.Д., Токсикологическая химия – 3-е изд., испр. – Москва «Медицина», 1975. – 376 с.;
7. http://lib.web-malina.com/getbook.php? bid=4141;
8. http://www.eurolab.ua/ru/encyclopedia/urgent.medica.aid/342/2466/;
9. http://www.test-poloska.ru/catalog/teststripes/ketophan.html;
10. http://www.xumuk.ru/toxicchem/ (В.Ф. Крамаренко-Токсикологическая химия);