Судово-медична діагностика раптової кардіальної смерті за допомогою комплексу лабораторних досліджень
СОДЕРЖАНИЕ: Дослідження провідної системи серця. Концепція застосування комплексу морфологічних, імуногістохімічних, імунологічних критеріїв для судово-медичної диференційної діагностики. Співвідношення кількості випадків смерті від ССЗ у залежності від статі.МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВЯ УКРАЇНИ
НАЦІОНАЛЬНА МЕДИЧНА АКАДЕМІЯ ПІСЛЯДИПЛОМНОЇ
ОСВІТИ імені П.Л. ШУПИКА
Мішин Михайло Юрійович
УДК 616 – 079.6 – 091.818
Cудово-медична діагностика раптової кардіальної смерті за допомогою комплексу лабораторних досліджень
14.01.25 - судова медицина
Автореферат дисертації на здобуття наукового ступеня
кандидата медичних наук
Київ – 2008
Дисертацією є рукопис
Робота виконана в Харківському національному медичному університеті МОЗ України
Науковий керівник:
доктор медичних наук, професор Ольховський Василь Олексійович, Харківський національний медичний університет, завідувач кафедри судової медицини та основ права імені Заслуженого професора УРСР М.С. Бокаріуса
Офіційні опоненти:
доктор медичних наук, професор Михайличенко Борис Валентинович, Національний медичний університет імені О.О. Богомольця, завідувач кафедри судової медицини
кандидат медичних наук, доцент Сулоєв Костянтин Миколайович, Дніпропетровська державна медична академія, доцент кафедри патологічної анатомії та судової медицини
Захист відбудеться “5” червня 2008р. о 1200 годині
на засіданні спеціалізованої вченої ради Д 26.613.03 при Національній медичній академії післядипломної освіти імені П.Л. Шупика (м. Київ) МОЗ України за адресою: 04112, м. Київ, вул. Оранжерейна, 9
З дисертацією можна ознайомитись у бібліотеці Національної медичної академії післядипломної освіти імені П.Л. Шупика (м. Київ) МОЗ України за адресою: 04112, м. Київ, вул. Дорогожицька, 9
Автореферат розісланий “11” квітня 2008р.
Вчений секретар
спеціалізованої вченої ради,
кандидат медичних наук
О.О. Гуріна
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИ
Актуальність теми. Проблема судово-медичної діагностики раптової кардіальної смерті (РКС), обумовленої серцево-судинними захворюваннями (ССЗ), у теперішній час є обєктом численних досліджень, що пояснюється поширеністю цієї патології. У даний час ССЗ продовжують залишатися головною причиною смертності в багатьох розвинених країнах (Зербіно Д.Д., Малик О.Р., 2004).
На основі комплексного морфологічного дослідження провідної системи серця були отримані нові дані стосовно гістологічної будови основних структурних елементів провідної системи (Грицина І.В., 2001). Додаткові діагностичні показники, що дозволяють посмертно констатувати патологію, прояви якої метаболічні, а не морфологічні, у даний час відсутні.
У теперішній час відбулася переоцінка ключових положень патогенезу ССЗ з позиції розвитку імунного запалення в судинній стінці. Велику роль у формуванні аутоімунних процесів при серцево-судинних захворюваннях відіграє порушення балансу цитокінів. На сучасному етапі отримані неспростовні докази того, що у розвитку запального процесу, особливо його гострої фази, беруть участь адаптогенні системи всього організму, й, насамперед, імунна, ендокринна та серцево-судинна (Ардаманський Н.А., Абакумова Ю.В., 1998). Імунні порушення відіграють важливу роль у виникненні патологічних станів при РКС (Гиязов З.А, 1977; Хромова А.М., 1998).
Доведено, що в міокарді при атеросклеротичній хворобі серця (АХС) має місце активна інфільтрація тканини циркулюючими в крові моноцитами та нейтрофілами. Активовані нейтрофіли посилюють утворення супероксид - радикалів і активізують перекисне окислення білків та ліпідів (ПОЛ). Підвищене виникнення вільних радикалів при дефіциті антиоксидантів стає патологічно значущим і супроводжується порушенням функціональних характеристик міоцитів (Абакумова Ю.В., Ардаманський Н.А., 2005).
З огляду на сучасне положення в області судово-медичної експертної практики, найбільш актуальними є дослідження в області діагностики РКС з різних причин. Це підкреслює важливість і першочергове значення інтенсифікації наукових досліджень з проблеми диференціального розмежування РКС. За останні часи за даною проблемою була проведена дослідницька робота стосовно судово-медичної оцінки змін регіонарних лімфатичних вузлів серця при гострій ішемічній хворобі серця (Мішалов В.Д., Сулоєв К.М., 2003).
При судово-медичному дослідженні нерідко бувають випадки конкуруючих причин смерті. У вивченій літературі, щодо актуальності цієї проблеми, зустрічаються окремі роботи, в яких фахівці намагалися вирішувати питання диференціальної діагностики при РКС (Хромова А.М., Забусов Ю.Г., 1998). Так, було проведено оцінку концентрації рівнів імуноглобулінів у сироватці крові. Зміна вмісту імуноглобулінів трупної крові разом з іншими даними може бути використана для вирішення питань, повязаних із раптовою смертю (Костилєв Д.В., 2003).
Враховуючи сучасне становище в галузі судово-медичної експертної практики, найбільш актуальними є дослідження диференційної діагностики РКС, що обумовлена ССЗ. Таким чином, можна зробити висновок про необхідність проведення досліджень у напрямку виявлення обєктивних і достовірних критеріїв судово-медичної діагностики РКС, обумовленої ДКМП, АКМП, АХС, гострим інфарктом міокарду без гемоперикарду (ГІМБГ).
Зв’язок роботи з науковими програмами, планами, темами.Дисертаційна робота є фрагментом планової науково-дослідної тематики Харківського національного медичного університету “Вивчення загальних закономірностей патологічних процесів та розроблення принципів і методів їх корекції”; теми основного плану кафедри судової медицини та основ права імені Заслуженого професора УРСР М.С. Бокаріуса ХНМУ: “Вивчення достовірності висновків експерта про причину смерті у випадках судово-медичної діагностики алкогольної кардіоміопатії” (державний реєстраційний номер 0106U001635), у виконанні якої дисертантом особисто проведені дослідження морфологічних, морфометричних ознак та імуноморфологічне обґрунтування застосування діагностичного алгоритму при РКС, що обумовлена АКМП, ДКМП, АХС, ГІМБГ. Тема дисертації затверджена Вченою Радою Харківського державного медичного університету 15 квітня 2004 року (протокол № 4).
Мета і завдання дослідження. Метою дослідження є підвищення ефективності діагностики РКС, що обумовлена ССЗ, на підставі розробки достовірних критеріїв судово-медичної діагностики РКС з урахуванням морфологічних, імунологічних, біохімічних показників. Виходячи з поставленої мети, визначено такі основні завдання дослідження:
1. Провести статистичний аналіз динаміки РКС за даними відділу №2 ХОБСМЕ за 2001-2006рр., визначити середній показник смертності від ССЗ порівняно з даними по Україні;
2. Описати обєктивні характерні морфологічні критерії при РКС, обумовленій ССЗ;
3. Вивчити імуногістохімічні особливості змін в міокарді осіб, смерть яких настала раптово від АХС, ГІМБГ, АКМП, ДКМП;
4. Визначити імунний статус (стан Т- і В-систем лімфоцитів, цитокіновий баланс) при РКС, оцінити вірогідність розходжень визначенних показників при РКС від АХС, ГІМБГ, ДКМП, АКМП;
5. Визначити й оцінити стан АОС і ПОЛ та рівень ендогенної інтоксикації при РКС від АХС, ГІМБГ, ДКМП, АКМП;
6. Розробити концепцію застосування комплексу морфологічних, імуногістохімічних, біохімічних, імунологічних критеріїв для судово-медичної диференційної діагностики РКС від АХС, ГІМБГ, ДКМП, АКМП.
Об’єкт дослідження – судово-медична діагностика РКС від АХС, ДКМП, АКМП, ГІМБГ.
Предмет дослідження – морфологічні ознаки та лабораторні показники РКС від АХС, ГІМБГ, ДКМП, АКМП, акти судово-медичного дослідження.
Методи дослідження: судово-медичні, морфологічні, гістологічні, імунологічні, імуногістологічні, біохімічні, мікроскопічні, статистичні.
Наукова новизна одержаних результатів. На регіональному рівні показано, що РКС займає перше місце серед ненасильної смертності. Вперше розроблені достовірні критеріі диференційної діагностики РКС, обумовленій ССЗ, на основі морфологічних та імунометаболічних показників, що дало можливість встановити рівень порушення імунного статусу, особливості клітинного метаболізму та морфогенезу при АХС, ГІМБГ, ДКМП, АКМП. Вивчено й описано особливості імунного, цитокінового та метаболічного статусу, характерні для РКС, обумовленій АХС, ГІМБГ, ДКМП, АКМП. Вперше запропоновано комплекс діагностичних критеріїв для диференціації різних форм РКС в судово - медичній практиці. Все визначене дозволило, сумісно з даними морфологічного дослідження, вперше запропонувати концепцію застосування вагомих достовірних показників для визначення комплексу діагностичних критеріїв щодо будування алгоритму диференціації різних форм РКС для підвищення ефективності судово-медичної діагностики РКС від АХС, ГІМБГ, ДКМП, АКМП.
Практичне значення одержаних результатів. На основі проведених досліджень розроблені практичні рекомендації щодо удосконалення судово-медичної диференційної діагностики різних форм РКС, що дозволить покращити якість судово- медичної діагностики. Для диференціальної діагностики РКС, що обумовлена ССЗ, рекомендується використовувати алгоритм проведення судово-медичного дослідження за допомогою лабораторних методів діагностики: проводити диференціацію РКС від ДКМП і АКМП за такими лабораторними показниками: визначення імунологічних критеріїв - CD8, CD21, TNF, IL-1, IL-4, клітинного цитокіну з дозозалежною активністю TGF-, метаболічних показників - ЛДГ, МДА, ДК, каталази, SH-груп у міокарді, МДА, ДК, каталази у сироватці крові, рівню ендогенної інтоксикації - МСВ у плазмі крові, що є достовірними для розмежування цих видів смерті; проводити диференціацію РКС від АХС і ГІМБГ на підставі достовірних критеріїв, що є CD8, NK, сіромукоїди, TNF, IL-6, IL-4, ЛДГ, МДА, ДК, каталази у сироватці крові та ЛДГ, МДА, ДК, каталази у міокарді, а також визначення відносних обємів лімфоцитів і клітин-продуцентів цитокінів у міокарді.
Визначений комплекс імунопатогенетичних причин РКС від АХС, ГІМБГ, ДКМП, АКМП розширює уяву про виникнення патологічних станів, що призводить до РКС. Алгоритм застосування діагностичних критеріїв при диференціації РКС впроваджено в навчальний процес, лекційні курси та практичні заняття кафедр судової медицини та основ права імені засл. проф. УРСР М.С. Бокаріуса й патологічної анатомії ХНМУ та у практичну діяльність Харківського обласного бюро судової медицини та Дніпропетровського ОКЗ «Бюро судово-медичної експертизи».
Особистий внесок здобувача. Автор самостійно здійснив пошук і аналіз літературних джерел. Ідею, напрямок досліджень, мету та завдання було обрано безпосередньо з науковим керівником доктором медичних наук, професором В.О. Ольховським. Самостійно обрано методологічні підходи, згідно з якими виконано дослідження з оцінки морфологічних, імуногістохімічних та метаболічних досліджень. Самостійно оброблено та проведено аналіз реєстрів розтинів за 2001 – 2006 рр. Автором самостійно проведено судово-медичну експертизу трупів осіб, що загинули від різних форм РКС, самостійно забрано матеріал для дослідження, проведено дослідження по вивченню морфологічних ознак при різних формах РКС. Самостійно досліджено та проаналізовано ефективність застосування лабораторних показників при різних формах РКС. Автором було проведено аналіз імунометаболічних досліджень та узагальнення одержаних лабораторних результатів. Всі положення, висновки, статистична обробка одержаних результатів належать пошукувачу.
Апробація результатів дисертації. Результати досліджень, що викладені у дисертації, доповідались на V Міжнародному конгресі з інтегративної антропології (Вінниця, 2004); Міжнародній науково-практичній конференції судових медиків та криміналістів «Актуальні питання та перспективи розвитку судової медицини та криміналістики» (Харків, 2005); Науково-практичній конференції з міжнародною участю, присвяченій 200–річчю з дня заснування ХДМУ «Від фундаментальних досліджень – до прогресу в медицині» (Харків, 2005); Міжвузівських конференціях молодих вчених «Медицина третього тисячоліття» (Харків, 2006, 2007рр); ІІ Національному конгресі з імунології «Сучасні досягнення клінічної імунології й алергології» (Київ – Миргород, 2007).
Публікації. За матеріалами дисертації опубліковано 9 наукових робіт, з них 3 статті у фахових виданнях, рекомендованих ВАК України (2 самостійні), 6 робіт – у матеріалах і тезах конгресів, з`їздів і конференцій (1 з них самостійна).
Структура та обсяг дисертації. Дисертація написана українською мовою та складається із вступу, огляду літератури, опису матеріалів й методів досліджень, 5 розділів власних досліджень, розділу аналізу і узагальнення результатів, висновків, практичних рекомендацій, списку використаних джерел. Повний обсяг дисертації – 137 сторінок. Робота має 16 таблиць, 15 рисунків та 22 фотографії. Список використаної літератури включає 136 джерел, з них вітчизняних і російських – 114, опублікованих за кордоном – 22.
ОСНОВНИЙ ЗМІСТ
Матеріали і методи дослідження. Матеріалом для судово-медичного дослідження були: зразки сироватки крові та фрагменти міокарду осіб, що загинули, від РКС, обумовленої АХС (20 випадків), АКМП (20 випадків), ДКМП (20 випадків), ГІМБГ (20 випадків). Контрольна група – зразки сироватки крові та фрагменти міокарду осіб, що померли від механічної травми – 20 випадків.
Морфологічні та гістологічні дослідження виконані за загальноприйнятими методами (Автанділов Г.Г., 1999; Герасименко О.І., Гаврик О.С., 1996; Лілі Р., 1969; Оболонський Н.А., 1994; Сапожніков А.Г., 2000).
Імунологічні дослідження проведені за методикою визначення субпопуляцій Т- та В- лімфоцитів периферичної крові з використанням МКАТ у РІФ; рівні СРБ та цитокінів визначали ІФА (Караулов А.В., 2002). Імуноморфологічне дослідження виконано з використанням непрямого методу Кунса. Типовано основні клони імунотропних клітин: загальна популяція Т-лімфоцитів (CD3+), Т-хелпери (CD4+), Т-цитотоксичні лімфоцити (CD8+), В-лімфоцити (CD21+), NK-клітини, клітини-продуценти цитокінів (Автанділов Г.Г., 1999). Для оцінки ступеня метаболічних порушень у крові та міокарді, обрано показники, які характеризують рівень енергетичного обміну (лактатдегідрогенази (ЛДГ), активність процесів ПОЛ: малоновий діальдегід (МДА), дієнові кон’югати (ДК) та стан антиоксидантної системи (АОС): вміст сульфгідрильних груп (SH) та каталази. Оцінку ступеня ендогенної інтоксикації проводили спектрофотометрично: визначали вміст молекул середньої ваги (МСВ) у плазмі крові. Облік і аналіз отриманих результатів проведено за допомогою автоматичного аналізатора «MULTISKAN EX». (Конторщикова К.Н., 2000). Одержані результати досліджень оброблено методом варіаційної статистики з використанням статистичної програми «BIOSTAT» (Лапач С.Н., 2000; Осипов В.П., 2002).
Результати власних досліджень та їх обговорення. За результатами статистичного аналізу РКС за даними відділу №2 ХОБСМЕ за 2001 – 2006 роки (рис. 1) спостерігається висока смертність від ССЗ (82,4 - 94,2%).
За даними архіву відділення № 2 відділення експертизи трупів ХОБСМЕ в 2001-2006 рр. РКС склала 86,80% (рис.2).
Що стосується аналізу даних випадків раптової смерті від ССЗ захворювань, то перше місце займає смертність від АХС – 63,9%; кардіоміопатії: АКМП – 18,8%, ДКМП – 0,6%); ГІМБГ – 1,8%; інші (перикардит, післяінфарктний кардіосклероз, коронарокардіосклероз, тощо) - 9,1%; ГХ – 5,8% (рис. 3).
Спостерігаючи динамічну картину смертності від ССЗ щодо співвідношення статі та віку померлих, можна констатувати той факт, що чоловіки гинуть у 2 рази частіше, ніж жінки, фактично незалежно від віку. За період 2001-2006 роки було 2048 випадків РКС від ССЗ серед жінок, що склало 33,2% та 4125 випадків РКС від ССЗ серед чоловіків, що склало 66,8%. Порівнюючі щорічні показники смертності залежно від статі видно, що у 2001 смертність від ССЗ у чоловіків перевищувала жіночу у 1,46 рази, у 2002 році – 2,2 рази, у 2003 - 2004 роках у 2 рази, у 2005 році – у 2,2 рази, у 2006 році – 2,3 рази, що ілюстративно наведено на рис. 4.
З метою зясування особливостей кількісного показника смерті від ССЗ проводили визначення показника смертності на 1000 відповідного населення, яке обслуговується теріторіально відділом №2 ХОБСМЕ. Згідно статистичних даних відділ №2 ХОБСМЕ обслуговує територію на якій мешкає 626089 людей. Таким чином, середній показник смертності по регіону, що обслуговує відділ №2 ХОБСМЕ склав 1,64 ‰.
У дисертації було досліджено морфологічні особливості РКС від ССЗ. При проведенні морфологічного дослідження РКС, що обумовлена ГІМБГ, ДКМП, АКМП, АХС, було встановлено наступні факти: РКС від АХС характеризувалась наявністю ознак атеросклерозу коронарних артерій, в міокарді – кардіосклерозом. При РКС, обумовленій ГІМБГ, спостерігалась вялість, блідність, іноді набряк міокарду в ділянці ішемії, гістологічно – запальні зміни в стінці магістральних гілок коронарних артерій, набряк інтими. При РКС від АКМП макроскопічно – помірна гіпертрофія серця, під епікардом виявлялось підвищене скупчення жирової клітковини, міокард вялий, гістологічно: жирова дистрофія та фрагментація кардіоміоцитів. При РКС, обумовленій ДКМП спостерігалась нерівномірна гіпертрофія серцевого мязу, гістологічно: нерівномірна атрофія кардіоміоцитів, дифузний міжм`язовий склероз, незначна інфільтрація строми лімфоїдними елементами. Для встановлення диференційного діагнозу між різними формами РКС, а саме від ДКМП, АКМП, ГІМБГ, АХС необхідно провести ряд лабораторних досліджень, що підтвердять або виключать причину смерті.
Міжклітинна сигналізація в імунній системі здійснюється безпосередньо за рахунок контактних взаємовідношень клітин з антигеном, шляхом активації поверхневих молекул (CD-маркерів) та за допомогою “білків зв’язку” – цитокінів. З атеросклерозом пов’язані: СРБ, проатерогенний медіатор IL-1, TNF-. Антиатерогенними властивостями володіють IL-4, TGF . Тому одним із завдань нашого дослідження було вивчення імунного та цитокінового статусу при РКС від ГІМБГ, АХС, ДКМП. Первинний ГІМБГ характеризувався зниженням кількості загальних Т-клітин (CD3), Т-супресорів (CD8). У трупів осіб, померлих від АХС, було виявлено зниження вмісту в крові кількості Т-лімфоцитів (CD3, CD8), а кількість В-лімфоцитів - відповідала показникам контрольної групи, що призводило до дисбалансу регуляторного індексу.
При РКС, внаслідок ГІМБГ та АХС, встановлено достовірне підвищення концентрацій IL-1, IL-4, IL-6 та TNF-a порівняно з контрольною групою (р0,001). При ДКМП концентрація IL-4 не відрізнялась від контрольної групи, при АКМП рівень його знизився (табл.1, 2).
Таблиця 1
Показники імунного статусу при РКС
| Показник | Контрольна група (n=20) |
Причина РКС | |||
ГІМБГ (n=20) |
АХС (n=20) |
АКМП (n=20) |
ДКМП (n=20) |
||
| СРБ мг/л | 1,8±0,3 | 11±1,6 * | 12±1,9 * | 4± 1,2 | 7±1,4* |
| CD3 % | 71,7±2,1 | 58+2,4* | 62±2,1** | 69±2,2 | 68±2,3 |
| CD4 % | 42±1,4 | 36± 1,5** | 39±1,4 | 42±1,2 | 41±1,6 |
| CD8 % | 35,5±1,9 | 27± 2,5* | 17±2,3* | 31±1,9 | 26±1,6* |
| CD21 % | 13,5±1,8 | 12± 1,7 | 11±1,9 | 10±1,6 | 7±1,5** |
| NK % | 14,5±1,7 | 14±1,5 | 24±2,1* | 16±1,9 | 14±1,7 |
| Серомукоїди у.о. | 0,165±0,02 | 0,057±0,01* | 0,134±0,02 | 0,215±0,04 | 0,106±0,02# |
*р0,001, ** р0,01, # р0,05 порівняно з контрольною групою осіб, що загинули від механічної травми.
Імуногістохімічно в міокарді при ГІМБГ визначено наступні клітини-продуценти: CD3, CD4, CD8 – Т-лімфоцити, CD21 - В-лімфоцити, макрофаги, моноцити, плазмобласти з IgM й IgG. Значно підвищеною була кількість клітин-продуцентів IL-1, IL-6, TNF. У серці при ДКМП, як і при АКМП, мали місце лімфогістіоцитарні інфільтрати, що локалізувалися периваскулярно та не поширювалися на суміжні відділи строми міокарду. У складі інфільтрації, також, як і при ГІМБГ, але в незначній кількості типували CD3, CD4, CD8 – Т-лімфоцити, CD21, макрофаги, моноцити, NK-клітини.
Таблиця 2
Показники цитокінового статусу при РКС
Показник пг/мл |
Контрольна група (n=20) |
Причина РКС | |||
| ГІМБГ (n=20) | АХС (n=20) | АКМП (n=20) | ДКМП (n=20) | ||
| TNF- | 42,57±2,5 | 91,5±5,6* | 73,5±2,3* | 57,23±2,4* | 48,2±2,1 |
| IL-1 | 27,67±1,3 | 48,2±2,9* | 47,8±2,1* | 37,63±1,4* | 31,63±1,8 |
| IL-6 | 39,96±2,1 | 99,7±1,9* | 73,6±1,9* | 43,21±1,9 | 40,1±1,9 |
| IL-4 | 43,11±3,4 | 86,16±4,2* | 64,2±2,5* | 38,9±1,5 | 45,23±1,9 |
| TGF | 18,2 ±09 | 3,22 ±0,6* | 2,6 ±0,3* | 16,3 ±1,2 | 20,8 ±1,4 |
*р0,001 порівняно з контрольною групою людей, що померли від механічної травми.
Серед елементів інфільтрації значно зменшилась доля макрофагів, клітин-продуцентів прозапальних цитокінів й збільшилась доля плазмобластів. Ендотеліоцити десквамовані, середній показник інтенсивності світіння ендотеліоцитів судин серця має тенденцію до зниження порівняно з такою при АХС, де у стромі і судинах серця виявились поодинокі клітини, що експресують рецептори до ED1, а також інтерлейкінам - IL-1, IL-6, TNF . В стромі міокарду визначено інтерстіціальні колагени І і ІІІ типів.
При РКС від АХС, ГІМБГ, АКМП, ДКМП у судинах серця чітко виражені базальні мембрани, на яких розташовані ендотеліоцити, що експресують рецептори до ендотеліну. Усереднений показник ступеня світіння ендотеліоцитів при кожній нозологічній одиниці відрізнявся від контрольної групи і був підвищений (рис 5).
Таким чином, дані мікроскопічного дослідження міокарду при АХС і ГІМБГ показують, що в ньому переважають явища розладу кровообігу, дистрофічні зміни й виражена запальна реакція в стромі, порівняно з контрольною групою. При ДКМП і АКМП системного ушкодження з боку інтерстіціальної тканини, а також стінок судин міокарду – не виявлено.
Одним з цитокінів, що обумовлюють розвиток аутоімунних процесів в організмі є TGF- (рис.6). При дії TGF- на імунну систему переважають інгібуючі ефекти, але він посилює синтез білків міжклітинного матриксу. Таким чином, TGF- є елементом зворотної регуляції імунної відповіді. За результатами наших досліджень рівень TGF- при РКС від АХС і від ГІМБГ зменшився у 7 та 5,7 рази відповідно порівняно з групою контролю.
Таким чином, активація прозапальних цитокінів (TNF, IL-1, IL-6) супроводжується підвищенням рівня протизапального цитокіну IL-4, окрім РКС від АКМП. Підвищення концентрації цитокінів у сироватці крові є свідченням активного системного запалення у судинній стінці при АXС та ГІМБГ.
Було досліджено особливості стану АОС та ПОЛ при різних формах РКС. На сучасному етапі доведено, що у міокарді при АХС має місце активна інфільтрація тканин циркулюючими у крові моноцитами та нейтрофілами. Активовані нейтрофіли посилюють утворення супероксид-радикалів і активують перекисне окислення білків і ліпідів.
Як показали результати проведених досліджень у міокарді осіб, що загинули від РКС, від АХС, підвищена активність процесів ПОЛ (вміст МДА збільшився у 1,7 рази, а ДК – у 2,9 рази порівняно з контрольною групою). Вміст SH-груп й активність каталази - зменшені, таким чином у міокарді має місце окислювальний стрес. Підвищується активність ЛДГ – ферменту анаеробного гліколізу, що свідчить про енергодефіцитний стан у міокарді (табл.3).
Вміст SH-груп у міокарді при РКС від АХС, ГІМБГ, АКМП, ДКМП знижується порівняно з контрольною групою, це свідчить про порушення активації антиоксидантної системи й про наявність оксидативного стресу в тканині міокарду при РКС (рис. 7).
При біохімічному дослідженні сироватки крові встановлено, що при РКС, обумовленій ДКМП, у 3 рази зростає вміст первинного продукту ПОЛ - ДК, у 1,8 рази збільшується вміст кінцевого продукту ПОЛ - МДА. При РКС, обумовленій ГІМБГ й АХС, спостерігається активація первинних і кінцевих продуктів ПОЛ: ДК у 4,3 і 2,4 рази та МДА у 2,4 і 1,5 рази відповідно. Зміни біохімічних показників, що вивчались, свідчать про порушення метаболізму.
Таблиця 3
Показники ПОЛ при РКС
| Показник | КГ (n=20) |
Причина РКС | ||||||||
| АХС (n=20) | ГІМБГ (n=20) | ДКМП (n=20) | АКМП (n=20) | |||||||
| сироватка крові | міо кард |
сироватка крові | міо кард |
сироватка крові | міо кард |
сироватка крові | міо кард |
сироватка крові | міо кард |
|
ЛДГ, мккат/л ммоль/хв·г білка |
30 ±1,2 |
27,3 ±0,9 | 33,7 ±0,8 |
35,7 ±0,7* |
39,9 ±0,8* |
42,8 ±0,6* |
35,9 ±0,9* |
39,3 ±0,9* |
33,7 ±0,7 |
29,7 ±0,8# |
МДА мкмоль/л мкмоль/г білка |
8,3 ±0,9 |
10,2 ±0,9 | 12,9 ±0,9* |
17,3 ±0,7* |
19,8 ±0,8* |
19,9 ±0,8* |
14,8± 0,8* |
19,8 ±0,6* |
10,2 ±0,7 |
14,9 ±0,6* |
ДК, мкмоль/л мкмоль/г білка |
1,6 ±0,4 |
1,8 ±0,8 |
3,9 ±0,6* |
5,3 ±0,4* |
6,9 ±0,9* |
7,8 ±0,5* |
4,8 ±0,7* |
7,1 ±0,7* |
2,7 ±0,6 |
3,4 ±0,6 |
Каталаза мккат/гНв ммоль/хв·г білка |
12,9 ±1,2 |
22,9 ±1,3 |
8,2 ±0,8* |
10,2 ±0,7* |
5,4 ±0,6* |
6,8 ±0,5* |
6,5 ±0,7 * |
7,5 ±0,5* |
10,6 ±0,9 |
15,8 ±0,9* |
| SH-групи, мМоль/л | - | 98 ±0,9 |
- | 51,9 ±0,8* |
- | 49,1 ±0,6* |
- | 66,13 ±1,3* |
- | 61,3 ±0,9* |
*р0,001, # р0,05, р0,02порівняно з контрольною групою (КГ) людей, що померли від механічної травми.
Таким чином, у міокарді осіб, що загинули від РКС, підвищений рівень ПОЛ при зниженні активності АОС, в тканині серця має місце окислювальний стрес, який призводить до розвитку енергодефіцитного стану, про що свідчить підвищення активності ЛДГ.
Дослідження синдрому ендогенної інтоксикації при РКС від ССЗ мало відомо. Показано, що ендотоксемія розвивається при всіх патологічних станах, пов`язаних з підвищенням катаболізму або блокадою детоксикаційних систем організму. Першим субстратом, що відповідає за виникнення патологічних ефектів ендогеної інтоксикації при патологічних станах, вважали білкові токсини –молекули середньої ваги (МСВ), що утворюються в процесі протеолізу в ушкоджених тканинах, а також у плазмі при виході в кров протеолітичних ферментів.
Накопичення МСВ не тільки є маркером ендоінтоксикації, і подальше вони поглиблюють перебіг патологічного процесу. МСВ володіють нейротоксичною активністю, пригнічують процеси біосинтезу білка, здатні пригнічувати активність ряду ферментів, , змінюють транспорт іонів через мембрани, фагоцитоз, мікроциркуляцію, лімфодинаміку, викликають стан вторинної імунодепресії.
При біохімічному дослідженні плазми крові встановлено, що при РКС, обумовленій АХС, ГІМБГ, значно збільшується (у 15,8 та 13,6 рази відповідно) рівень МСВ, а при РКС, обумовленій ДКМП у 4,8 рази підвищується МСВ порівняно з контрольною групою (рис. 8). При АКМП практично не збільшується вміст МСВ порівняно з контрольною групою.
Таким чином, проведені дослідження свідчать про активацію вільнорадикальних процесів при РКС, що пов’язано з пригніченням АОС у зв’язку з активацією (стимуляцією) механізмів запалення й аутоімунних реакцій у тканині міокарда при ДКМП і судинах при АХС.
Для розробки алгоритму проведення диференціальної діагностики РКС, обумовленої ГІМБГ, ДКМП, АКМП, АХС, нами проведено узагальнення отриманих результатів досліджень. Патофізиологічним підґрунтям концептуальної моделі диференційної діагностики окремих видів РКС є імунопатологічний механізм інгібіції клітинної ланки імунітету, що призводить до системного обмінного дисбалансу, в якому імунний, цитокіновий та метаболічний стан організму та серцевого мязу з позиції активації вільнорадикальних процесів ПОЛ призводить до накопичення активних форм кисню, перекисей, вільних радикалів, які руйнують структуру біологічних мембран міокардіоцитів, модулюючи вільнорадикальну патологію. Тривала стимуляція ПОЛ призводить до виснаження АОС, інгібування процесів біоенергетики й пригнічення біосинтетичних процесів у цілому. Ці процеси є визначними в формуванні морфологічних змін у серцевому мязі. Тому використання комплексного лабораторного дослідження, яке базується, передусім, на зясуванні імунного, цитокінового та метаболічного стану організму та серцевого мязу надасть можливість диференціації конкуруючих причин смерті.
Концепція застосування комплексу лабораторних досліджень для диференційної діагностики РКС, обумовленої АХС, ГІМБГ, ДКМП, АКМП передбачає врахування даних патоморфологічного дослідження (макроскопічне дослідження серця та його судин з мікроскопічним та гістоімунологічним дослідженням міокарду), біохімічного (АОС/ПОЛ, рівень ендогенної інтоксикації) та імунологічного (імунний та цитокіновий статус), що представлено на рис. 10.
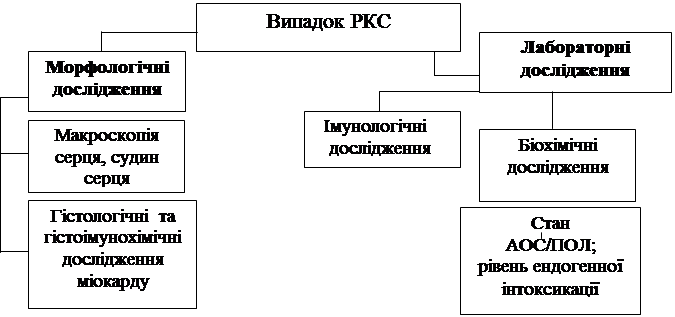
Рис. 10. Алгоритм застосування діагностичних критеріїв при диференціації РКС.
Враховуючи спільні механізми формування патології, нами проведено групування випадків РКС у дві групи: атеросклеротичного (АХС та ГІМБГ) і неатеросклеротичного (ДКМП та АКМП ) ураження.
Морфологічні дослідження. Як відомо, в судово-медичній експертизі з діагностичною метою досить активно використовують морфологічне – макро- та мікроскопічне дослідження. Проведене нами дослідження вказує, що за морфологічними ознаками – макроскопічними: вялість міокарду, кровонаповнення, вага серця, гіпертрофія серця та мікроскопічними: набряк інтими судин серця, фіброзно-тканинні бляшки, стан кардіоміоцитів, набряк строми, лейкоцитарна інфільтрація інтерстиції, стан коронарних судин - можливо визначити причину РКС. В той же час для глибокого розуміння як причини морфологічних змін, так і отримання диференційно діагностичних показників, важливо зясувати роль та місце обмінних порушень в міокарді та організмі.
Для імуногістохімічного розмежування РКС (табл. 4) з атеросклеротичним механізмом формування змін у міокарді - АХС та ГІМБГ діагностичне значення мають клітини – продуценти лімфоцитів, а також клітини-продуценти цитокінів (р0,05). Макрофагальну реакцію та реакцію плазмобластної трансформації не можливо вважати діагностичною, оскільки достовірної різниці між групами порівняння не спостерігається.
Для розмежування РКС з неатеросклеротичним механізмом формування змін у міокарді (АКМП і ДКМП) діагностичним критерієм може бути тільки наявність основних клонів клітин-продуцентів цитокінів (р0,05). Інші імуногістохімічні показники виявились не достовірними.
Таблиця 4
Визначення імуногістохімічних показників для диференціації РКС від ГІМБГ і АХС та РКС від АКМП і ДКМП
| Патогенетичне розмежування причин РКС | з атеросклеротичним ураженням | без атеросклеротичного ураження | ||
| показники | ГІМБГ | АХС | АКМП | ДКМП |
| лімфоцити | 55,0±2,0 | 61,0±2,0 | різниця не достовірна |
|
| р0,05 | ||||
| клітини- продуценти цитокінів | 39,0±1,0 | 42,0±1,0 | 21,0±1,0 | 18,0±1,0 |
| р0,05 | р0,05 | |||
Імунологічні дослідження. Для диференціації РКС з атеросклеротичним ураженням – АХС і ГІМБГ діагностично значущими імунологічними показниками є зміни вмісту Т-цитотоксичних лімфоцитів (CD8), NK-клітин, концентрації сіромукоїдів та цитокінів (TNF, IL-6, IL-4). Що ж стосується таких показників, як CD3 (загальна популяція Т-лімфоцитів), CD4 (Т-хелпери), CD21 (В-клітини), IL-1 (прозапальний цитокін) та TGF- (трансформуючий фактор росту), то їх зміни виявились недостовірними, а саме – діагностично не значними для розмежування РКС від АХС і РКС від ГІМБГ.
Для розмежування випадків РКС з неатеросклеротичним механізмом формування патології у міокарді (АКМП та ДКМП) діагностичними критеріями являються зміни вмісту Т-цитотоксичних лімфоцитів (CD8), В-клітин (CD21), цитокінів (TNF, IL-1, IL-4, TGF-), а такі показники, як CD3 (загальна популяція Т-лімфоцитів), CD4 (Т-хелпери), NK-клітини, сіромукоїди, IL-6 – не дозволяє провести їх розмежування між собою.
Визначені імунологічні діагностичні показники для диференціації РКС від ГІМБГ і АХС та РКС від АКМП і ДКМП наведені в таблиці 5.
Таблиця 5
Визначення імунологічних показників для диференціації РКС від ГІМБГ і АХС та РКС від АКМП і ДКМП
| Патогенетичне розмежування причин РКС | З атеросклеротичним ураженням | Без атеросклеротичного ураження | ||
| показники | ГІМБГ | АХС | АКМП | ДКМП |
| CD8, % | 27±2,5 | 17±2,3 | 31±1,9 | 26±1,6 |
| р0,01 | р0,001 | |||
| CD21, % | різниця не достовірна | 10±1,6 | 7±1,5 | |
| р0,05 | ||||
| NK, % | 14±1,5 | 24±2,1 | різниця не достовірна | |
| р0,001 | ||||
| Сіромукоїди, у.о | 0,057±0,01 | 0,134±0,02 | різниця не достовірна | |
| р0,001 | ||||
| TNF, пг/мл | 91,5±5,6 | 73,5±2,3 | 57,23±2,4 | 48,2±2,1 |
| р0,01 | р0,01 | |||
| IL-1, пг/мл | різниця не достовірна | 37,63±1,4 | 31,63±1,8 | |
| р0,01 | ||||
| IL-6, пг/мл | 99,7 ±1,9 | 73,6 ±1,9 | різниця не достовірна | |
| р0,001 | ||||
| IL-4, пг/мл | 86,6±4,2 | 64,2±2,5 | 38,9±1,5 | 45,2±1,9 |
| р0,001 | р0,01 | |||
| TGF-, нг/мл | різниця не достовірна | 16,3±0,8 | 20,8±1,3 | |
| р0,01 | ||||
Біохімічні дослідження. Діагностичними критеріями в тканині серця для диференціації РКС з атеросклеротичним механізмом формування змін у міокарді (АХС та ГІМБГ) є концентрації ЛДГ, МДА, ДК, каталази, а визначення SH-груп виявилось недостовірним. У сироватці крові діагностичними критеріями є вміст ЛДГ, МДА, ДК та каталази.
Показник ендогенної інтоксикації – МСВ є діагностичним критерієм для РКС з неатеросклеротичним механізмом формування змін в міокарді (АКМП і ДКМП), що доречно застосовувати для їх диференціації (табл. 6).
Таблиця 6
Визначення біохімічних показників для диференціації РКС від ГІМБГ і АХС та РКС від АКМП і ДКМП
| Патогенетичне розмежування причин РКС | з атеросклеротичним ураженням | без атеросклеротичного ураження | ||||
| показники | ГІМБГ | АХС | АКМП | ДКМП | ||
| Стан АОС/ПОЛ у міокарді | ||||||
| ЛДГ, ммоль/хв.г білка | 42,8±0,6 | 35,7±0,7 | 29,7±0,8 | 39,3±0,9 | ||
| р0,001 | р0,001 | |||||
| МДА, мкмоль/г білка | 19,9±0,8 | 17,3±0,7 | 14,9±0,6 | 19,8±0,6 | ||
| р0,02 | р0,001 | |||||
| ДК, мкмоль/г білка | 7,8±0,5 | 5,3±0,4 | 3,4±0,6 | 7,1±0,7 | ||
| р0,001 | р0,001 | |||||
| Каталаза, ммоль/хв.г білка | 6,8±0,5 | 10,2±0,7 | 15,8±0,9 | 7,5±0,5 | ||
| р0,001 | р0,001 | |||||
| SH-групи | різниця не достовірна | 61±1,8 | 66±1,8 | |||
| р0,05 | ||||||
| Стан АОС/ПОЛ у сироватці (плазмі) крові | ||||||
| ЛДГ, мккат/л | 39,9±0,8 | 33,7±0,8 | різниця не достовірна | |||
| р0,001 | ||||||
| МДА, мкмоль/л | 19,8±0,8* | 12,9±0,9* | 10,2±0,7* | 14,8±0,8* | ||
| р0,001 | р0,001 | |||||
| ДК, мкмоль/л | 6,9±0,9 | 3,9±0,6 | 2,7±0,6 | 4,8±0,7 | ||
| р0,01 | р0,05 | |||||
| Каталаза, мккат/г Нв | 5,4±0,6 | 8,2±0,8 | 10,6±0,9 | 6,5±0,7 | ||
| р0,01 | р0,001 | |||||
| Рівень ендогенної інтоксикації | ||||||
| МСВ, у.о | різниця не достовірна | 0,08±0,006 | 0,24±0,009 | |||
| р0,001 | ||||||
Диференціація РКС з неатеросклеротичним механізмом формування змін у міокарді (АКМП та ДКМП) має враховувати такі діагностичні показники в міокарді, як концентрація ЛДГ, МДА, ДК, каталази, SH-груп, а в сироватці крові - МДА, ДК, каталази. Що ж стосується серцевої фракції ЛДГ, то її зміни виявились недостовірними.
Таким чином, використання імунометаболічних показників дозволяє оптимізувати судово-медичну діагностику випадків РКС при атеросклеротичному ураженні міокарда (АХС та ГІМБГ) й неатеросклеротичному ураженні (АКМП та ДКМП) та обґрунтувати післямортальний діагноз з точки зору патофізіологічних процесів.
ВИСНОВКИ
У дисертації вперше вирішене актуальне завдання, що полягало у підвищенні ефективності судово-медичної діагностики РКС від АХС, ГІМБГ, АКМП, ДКМП з урахуванням морфологічних, імунологічних та біохімічних змін.
1. Середній показник смертності населення регіону, який обслуговує відділ №2 ХОБСМЕ, за період 2001-2006 рр, від ССЗ склав 1,64 на 1000 населення, що у 4 рази нижче за аналогічний показник по Україні, який дорівнював 6,56.
2. Морфологічні макро- та мікроскопічні зміни в міокарді осіб, РКС яких настала від атеросклеротичного (АХС, ГІМБГ) та неатеросклеротичного (АКМП, ДКМП) ураження, є показовими й вірогідними, а їх поява обумовлюється комплексом імунометаболічних порушень в організмі та серцевому мязі при цих захворюваннях, що може бути використано для обґрунтування причини РКС .
3. Морфологічні зміни в міокарді осіб, РКС яких настала від АХС, ГІМБГ, АКМП та ДКМП, різняться за своєю імуногістохімічною характеристикою.
Імуногістохімічно міокард при АХС характеризується наявністю малочислених нейтрофільних гранулоцитів, плазмоцитів з IgM та IgG, макрофагів, чисельними лімфоцитами й клітинами-продуцентами цитокінів, осередковим світінням колагену. У міокарді осіб, смерть яких настала від ГІМБГ, виявлено клітини–продуценти лімфоцитів, моноцити, підвищену кількість клітин-продуцентів інтерлейкінів. При РКС від АКМП виявлено переваскулярні лімфогістіоцитарні інфільтрати, поодинокі лімфоцити, а при ДКМП – NK-клітини в стромі міокарду, світіння ендотеліоцитів, макрофагальну реакцію та реакцію плазмобластної трансформації, прояви яких зменшені порівняно з контрольною групою.
Для імуногістохімічного розмежування РКС з атеросклеротичним механізмом формування змін у міокарді - АХС та ГІМБГ діагностичне значення мають клітини – продуценти лімфоцитів, а також клітини-продуценти цитокінів.
Для розмежування РКС з неатеросклеротичним механізмом формування змін у міокарді (АКМП і ДКМП) діагностичним критерієм може бути тільки наявність основних клонів клітин-продуцентів цитокінів.
4. Діагностично значущими імунологічними показниками крові при РКС з атеросклеротичним ураженням міокарду (АХС і ГІМБГ) є Т-цитотоксичні лімфоцити (CD8), NK-клітини, сіромукоїди, цитокіни (TNF, IL-6, IL-4), а при РКС з неатеросклеротичним ураженням міокарду (АКМП і ДКМП) - Т-цитотоксичні лімфоцити (CD8), В-клітини (CD21), цитокіни (TNF, IL-1, IL-4, TGF-).
5. Біохімічна диференціація РКС від АХС порівняно з ГІМБГ базується на виявленні у міокарді ЛДГ, МДА, ДК, каталази, в сироватці крові – ЛДГ, МДА, ДК, каталази; при диференціації РКС від АКМП порівняно з ДКМП враховують вміст у міокарді ЛДГ, МДА, ДК, каталази, SH-групи, в сироватці крові - МДА, ДК, каталази. Що ж стосується МСВ, то їх концентрація як показника ендогенної інтоксикації, дозволяє провести розмежування РКС від АКМП і ДКМП.
6. Використання комплексу імунометаболічних показників дозволяє оптимізувати судово-медичну діагностику випадків РКС при атеросклеротичному ураженні (АХС та ГІМБГ) й неатеросклеротичному ураженні (АКМП та ДКМП) міокарду.
ПРАКТИЧНІ РЕКОМЕНДАЦІЇ
За результатами проведеного дослідження для підвищення ефективності диференціальної діагностики РКС від АХС, ГІМБГ, АКМП, ДКМП пропонуємо для впровадження в практику судово-медичної експертизи окрім загальновідомих методів дослідження:
1.Для диференціальної діагностики РКС, що обумовлена ССЗ, використовувати алгоритм проведення судово-медичного дослідження за допомогою лабораторних методів діагностики.
2.Проводити диференціацію РКС від ДКМП і АКМП за такими лабораторними показниками: визначення CD8, CD21, TNF, IL-1, IL-4, клітинного цитокіну з дозозалежною активністю TGF-, ЛДГ, МДА, ДК, каталази, SH-груп у міокарді, МСВ у плазмі крові, що є достовірними для розмежування цих видів смерті.
3.Проводити диференціацію РКС від АХС і ГІМБГ на підставі достовірних критеріїв, що є CD8, NK, сіромукоїди, TNF, IL-6, IL-4, ЛДГ, МДА, ДК, каталази у сироватці крові.
4.Диференційна діагностика РКС від АХС, ГІМБГ, ДКМП, АКМП повинна здійснюватись шляхом комплексного використання патоморфологічних, гістологічних, імунологічних та біохімічних методів дослідження, що є доречним, об`єктивним і достовірним критерієм для офіційного висновку про причину смерті.
5. Визначений комплекс імунопатогенетичних причин РКС від АХС, ГІМБГ, ДКМП, АКМП розширює уявлення про виникнення патологічних станів, які призводять до РКС, що доречно впровадити в навчальний процес, лекційні курси та практичні заняття кафедр судової медицини та патологічної анатомії медичних ВУЗів України та в практичну діяльність судово-медичних експертів.
СПИСОК ОПУБЛІКОВАНИХ ПРАЦЬ ЗА ТЕМОЮ ДИСЕРТАЦІЇ
1. Мішин М.Ю. Особливості змін імунного профілю при раптовій кардіальній смерті // Український судово-медичний вісник. - 2006. - №2 (19). – С. 23 – 25.
2. Мішин М.Ю. Особливості процесів перекисного окислення при раптовій кардіальній смерті // Український судово-медичний вісник. - 2007. - №1 (20). – С. 40 – 42.
3. Ольховський В.А., Мишин М.Ю. Статистический анализ динамики кардиальной смертности по данным ХОБСМЭ №2 за 2001 – 2006 годы //Медицина сьогодні і завтра. - 2007. - № 3. – С. 75- 77. (Здобувачем проведено статистичний аналіз динаміки РКС за даними ХОБСМЕ №2 за період 2001 – 2006 рр.).
4. Ольховський В.О., Мішин М.Ю. Сучасний погляд на проблему судово-медичної діагностики нозологічних форм раптової смерті //V Міжнародний конгрес з інтегративної антропології, Вінниця, 3-4 червня 2004. - Biomedical and Biosocial Anthropology, 2004. - №2. – С.66. (Здобувачем проведено аналіз даної проблеми за оглядом сучасної літератури й викреслено аспекти діагностичних досліджень РКС).
5. Цыганенко А.Я., Ольховский В.А., Мишин М.Ю., Мишина М.М. Показатели цитокинового баланса при внезапной сердечной смерти//Матеріали науково-практичної конференції з міжнародною участю, присвяченої 200-річчю з дня заснування ХДМУ «Від фундаментальних досліджень до прогресу в медицині». Харків 17-18 січня, 2005. – Харків, 2005. - С. 68. (Здобувачем узагальнено результати проведених досліджень цитокінового стану при РКС від АХС, ГІМБГ, АКМП, ДКМП та проведено статистична оцінка розходження визначених показників).
6. Ольховский В.А., Мишин М.Ю. Антиоксидантный статус при внезапной кардиальной смерти, обусловленной атеросклеротической болезнью сердца //Матеріали міжнародної науково-практичної конференції судових медиків та криміналістів, присвяченої 200-річчю кафедри судової медицини та основ права ХДМУ «Актуальні питання та перспективи розвитку судової медицини та криміналістики». Харків, 14-16 вересня 2005. – Харків, 2005 – С. 168 – 169. (Здобувачем зібрано фактичний матеріал лабораторних досліджень антиоксидантної системи та стану перекисного окислення ліпідів при РКС та узагальнено результати дослідження).
7. Ольховский В.А. Мишин М.Ю., Вороной Ю.Ю., Карпенко В.А. Критерии цитокинового статуса при внезапной кардиальной смерти //Матеріали Першої міжнародної науково-практичної конференції судових медиків і криміналістів, присвяченої 75-річчю з дня смерті Заслуженого проф. М.С. Бокаріуса «Бокаріусовькі читання». Харків, 2006. – Харків, 2006. – С. 46 – 47. (Здобувачем зібрано фактичний матеріал лабораторних досліджень стану цитокінів при РКС від АХС, ГІМБГ, ДКМП, АКМП та узагальнено й статистично оброблено здобуті результати).
8. Мишин М.Ю. Статистический анализ динамики кардиальной смертности по данням отделения №2 ХОБСМЭ за 2001 – 2005 гг. //Медицина третього тисячоліття: зб.тез міжвузівської конференції молодих вчених та спеціалістів, Харків, 17-18 січня 2006. - С. 28.
9. Циганенко А.Я., Ольховський В.О., Мішин М.Ю., Мішина М.М., Кузьменко А.М. Імунні аспекти при раптовій кардіальній смерті // Національний конгрес з імунології, алергології та імунореабілітації на тему „Сучасні досягнення клінічної імунології й алергології”. Київ-Миргород 19-23 листопада, 2007. - Миргород. – С.82. (Здобувачем зібрано фактичний матеріал лабораторних досліджень стану імунної системи при РКС й узагальнено результати).
АНОТАЦІЯ
Мішин М.Ю. Судово-медична діагностика раптової кардіальної смерті за допомогою комплексу лабораторних досліджень. – Рукопис.
Дисертація на здобуття наукового ступеня кандидата медичних наук за спеціальністю 14.01.25 – судова медицина. – Національна медична академія післядипломної освіти імені П.Л. Шупика. – Київ, 2008.
Дисертація присвячена підвищенню ефективності діагностики РКС, що обумовлена ССЗ, на підставі розробки достовірних критеріїв судово-медичної діагностики даної патології з урахуванням морфологічних, імунологічних, біохімічних показників. На регіональному рівні показано, що РКС займає перше місце серед ненасильної смертності. Встановлено рівень порушення імунного статусу, клітинного метаболізму та морфогенезу. Вивчено й описано особливості імунометаболічного статусу, характерні для РКС. На основі імунологічних та біохімічних показників виявлено достовірні критерії диференційної діагностики РКС, обумовленої ССЗ. Запропоновано комплекс діагностичних критеріїв для диференціації РКС від ССЗ в судово-медичній практиці.
Ключові слова: раптова кардіальна смерть, серцево-судинні захворювання, діагностичні критерії, статистичний аналіз.
АННОТАЦИЯ
Мишин М.Ю. Судебно-медицинская диагностика внезапной кардиальной смерти с помощью комплекса лабораторных исследований. – Рукопись.
Диссертация на соискание научной степени кандидата медицинских наук по специальности 14.01.25 – судебная медицина. – Национальная медицинская академия последипломного образования имени П.Л. Шупика. – Киев, 2008.
Диссертация посвящена повышению эффективности диагностики внезапной кардиальной смерти (ВКС), обусловленной сердечно-сосудистыми заболеваниями, на основании разработки достоверных критериев судебно-медицинской диагностики данной патологии с учетом морфологических, иммунологических, биохимических показателей. На регионарном уровне показано, что ВКС занимает первое место среди ненасильственной смертности. Установлены уровни нарушения иммунного статуса, клеточного метаболизма и морфогенеза при ВКС, обусловленной атеросклеротической болезнью сердца (АБС), острым инфарктом миокарда без гемоперикарда (ОИМБГ), дилятационной кардиомиопатией (ДКМП), алкогольной кардиомиопатией (АКМП). Изучены, описаны и проанализированы особенности цитокинового баланса, при ВКС. Проведенные исследования позволили обобщить результаты и разработать алгоритм проведения дифференциальной диагностики ВКС от ОИМБГ, ДКМП, АКМП, АБС, который заключается в использовании комплекса показателей, входящих в концептуальную модель иммунопатологических механизмов, обуславливающих возникновение ВКС. Эта модель включает выявленные в процессе исследования достоверные критерии, которые рекомендуется использовать на этапах дифференциации конкурирующих причин ВКС. Концепция применения комплекса лабораторных исследований при дифференциальной судебно-медицинской диагностики ВКС, обусловленной АБС, ОИМБГ, ДКМП, АКМП, состоит из нескольких этапов: этап патоморфологического диагноза (макроскопические исследования сердца и сосудов сердца), этап гистологического диагноза (микроскопические исследования миокарда), этап определения лабораторных критериев, которые включают биохимические исследования (состояние антиоксидантной системы, перекисного окисления липидов, степень эндогенной интоксикации) и иммунологические показатели (исследование иммунного и цитокинового статуса). Это позволит повысить уровень эффективности судебно-медицинской диагностики ВКС.
Ключевые слова: внезапная кардиальная смерть, сердечно-сосудистые заболевания, диагностические критерии, статистический анализ.
SUMMARY
Mishin M. Yu. Forensic medical diagnostics of sudden cardiac death with the help of complex laboratory research. – Manuscript.
The thesis for scientific degree of Candidate of Medical Sciences, speciality 14.01.25– Forensic medicine. – P.L. Shupyk National Medical Academy of Post-Graduate Education. – Kiev, 2008.
The thesis is devoted to increasing the effectiveness of diagnostics of sudden cardiac death conditioned by cardiovascular diseases on the base of development of significant criteria in forensic medical diagnostics of such pathology considering morphological, immunological, biochemical indexes. It was shown on regional level that sudden cardiac death obtain first place between nonviolent mortality. The level of disturbance in immune status, cell metabolism and morphogenesis was determined. The properties of cytokine status in sudden cardiac death were studied and described. Significant indexes of differential diagnostics in sudden cardiac death conditioned by cardiovascular diseases were revealed on base of immunological and biochemical research. The complex of diagnostic criteria for differentiation the sudden cardiac death conditioned by cardiovascular diseases was recommended for using in forensic medical practice.
Key words: sudden cardiac death, cardiovascular diseases, diagnostic criteria, statistical analysis.