Термодинамический анализ цикла газовой машины
СОДЕРЖАНИЕ: Газовый цикл и его четыре процесса, определяемые по показателю политропы. Параметры для основных точек цикла, расчет промежуточных точек. Расчет постоянной теплоемкости газа. Процесс политропный, изохорный, адиабатный, изохорный. Молярная масса газа.Федеральное агентство по образованию
Архангельский государственный технический университет
Кафедра теплотехники
Специальность ОСП-ЭП Курс 1 Группа
Антошкин Евгений Валерьевич
КОНТРОЛЬНАЯ РАБОТА
по дисциплине: Теоретические основы теплотехники
(шифр – «наименование»)
на тему: Термодинамический анализ цикла газовой машины
Руководитель работы профессор С.В.Карпов
Оценка проекта (работы) ________________
Архангельск
2007
Федеральное агентство по образованию
Архангельский государственный технический университет
Кафедра теплотехники
ЗАДАНИЕ
КОНТРОЛЬНУЮ РАБОТУ
по дисциплине: Теоретические основы теплотехники
студенту ОСП-ЭП курса 1 группы Антошкину Евгению Валерьевичу
Тема: Термодинамический анализ цикла газовой машины
Исходные данные: Рабочее тело обладает свойствами воздуха, масса равна 1 кг
Газовый цикл состоит из четырех процессов, определяемые по показателю политропы. Известны начальные параметры в точке 1 (давление и температура), а также безразмерные отношение параметров в некоторых процессах
Дано:
n1-2 =1,35; n2-3 = ; n3-4 = К; n4-1 = ; p1 = 1105 Па; t1 = 90 C;
v1/v2 = 10; р3/р2 = 1,5.
Найти: параметры для основных точек цикла:pi, vi, ti, ui, ii, si,
Определить для каждого процесса: u, i, s, q, l, l*; = u/q; = l/q.
Определить работу газа за цикл lц, термическое к.п.д. и среднецикловое давление Pi.
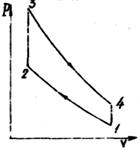
Построить в масштабе цикл в координатах P,v; T,S.
Расчет производится при постоянной теплоемкости.
Срок выполнения работы с__________2007г. по ___________2007г.
Руководитель проекта Карпов С.В.«___»_____________2007г.
Исходные данные :
| № вар-та | Показатель политропы | PI , 10-5 Па | t1 0 C | Расчетный цикл | |||||
| 1-2 | 2-3 | 3-4 | 4-1 | ||||||
|
28 |
1,35 |
К |
1,00 |
90 |
10 |
1,5 |
 |
||
Определим характеристики:
1-2 – политропный процесс,
2-3 – изохорный процесс,
3-4 – адиабатный процесс,
4-1 – изохорный процесс.
Дополнительные данные:
R=в =287Дж/кгК – газовая постоянная воздуха,
=29кг/кмоль – молярная масса газа,
Ср=Ср· / =74,187/29=1,01- теплоемкость газа,
Cv=Cv·µ/µ=5·4,187/29=0,722- теплоемкость газа,
k=Cp/Cv=7/5=1,4 - показатель Пуассона или показатель адиабаты.
Решение.
1 Определение параметров для основных точек цикла
Точка 1.
p1 v1 =RT1 ,
T1 =273+90=363 К.
v1 =RT1 /р1 =287363/1105 =1,042 м3 /кг.
u1 =cv T1 =0,722363=262,09 кДж/кг
i1 =cp T1 =1,01363=366,63 кДж/кг
s1 =cp ln(T1 /273) Rln (p1 /1,013)=1,01ln(363/273)–0,287ln (1/1,013)=0,291 кДж/(кгК)
Точка 2.
v2 =v1 /10= 0,104 м3 /кг.
p2 = p1 (v1 /v2 )n = 1105 (10)1,35 = 22,387105 Па
Т2 =р2 v2 /R= 22,387105 0,104/287=811 K
t2 = 811 – 273 = 538C
u2 = cv T2 = 0,722811= 585,54 кДж/кг
i2 = cp T2 = 1,01 811= 819,11 кДж/кг
s2 = cp ln(T2 /273) – Rln (p2 /1,013) = 1,01 ln(811/273) – 0,287ln (22,387/1,013) = 0,211 кДж/(кгК)
Точка 3.
р3 =1,5р2 =50,37105 Па
v2 = v3 =0,104 м3 /кг
Т3 =р3 v3 /R= 50,37105 0,104/287=1825 K
t3 = 1825 – 273 = 1552C
u3 = cv T3 = 0,7221825= 1317,65 кДж/кг
i3 = cp T3 = 1,01 1825= 1843,25 кДж/кг
s3 =cp ln(T3 /273)–Rln(p3 /1,013)=1,01ln(1825/273)–0,287 ln (50,37/1,013) = 0,798 кДж/(кгК)
Точка 4.
v4 =v1 =1,042 м3 /кг
p4 = p3 (v3 /v4 )k = 50,37105 (0,104/1,042)1,4 = 2,00105 Па
Т4 = р4 v4 /R= 2,00105 1,042/287 = 726 К.
t4 =726 – 273 = 453C
u4 = cv T4 = 0,722726= 524,17 кДж/кг
i4 = cp T4 = 1,01726 = 733,26 кДж/кг
s4 =cp ln(T4 /273)–Rln(p4 /1,013)=1,01ln(726/273,15)– 0,287ln (2,00/1,013) = 0,793 кДж/(кгК)
Таблица №1
| № точки | р, Па | v, м3/кг | t, С | T, К | u, кДж/кг | i, кДж/кг | s, кДж/(кгК) |
| 1 | 1,00105 | 1,042 | 90 | 363 | 262,09 | 366,63 | 0,291 |
| 2 | 22,387105 | 0,104 | 538 | 811 | 585,54 | 819,11 | 0,211 |
| 3 | 50,37105 | 0,104 | 1552 | 1825 | 1317,65 | 1843,25 | 0,798 |
| 4 | 2,00105 | 1,042 | 453 | 726 | 524,17 | 733,26 | 0,793 |
2 Определение u, i, s
1. Процесс 1 – 2.
u = u2 – u1 = 585,54 – 262,09 = 323,45 кДж/кг
i = i2 – i1 = 819,11 – 366,63 = 452,48 кДж/кг
s =s2 – s1 = 0,211 – 0,291 = -0,080кДж/кг
2. Процесс 2 – 3.
u = u3 – u2 = 1317,65 – 585,54 = 732,11 кДж/кг
i = i3 – i2 = 1843,25 – 819,11 = 1024,14 кДж/кг
s =s3 – s2 = 0,798 –0,211 = 0,587 кДж/кг
3. Процесс 3 – 4.
u = u4 – u3 = 524,17 – 1317,65 = - 793,48 кДж/кг
i = i4 – i3 = 733,26 – 1843,25 = - 1109,99 кДж/кг
s =s4 – s3 = 0,793 – 0,798 = - 0,005 кДж/кг
4. Процесс 4 – 1.
u = u1 – u4 = 262,09 – 524,17 = - 262,08 кДж/кг
i = i1 – i4 = 366,63 – 733,26 = -366,63 кДж/кг
s = s1 – s4 = 0,291 – 0,793 = -0,502 кДж/кг
Таблица №2
| № процессов | u, кДж/кг | i, кДж/кг | s, кДж/(кгС) |
| 1-2 | 323,45 | 452,48 | -0,080 |
| 2-3 | 732,11 | 1024,14 | 0,587 |
| 3-4 | - 793,48 | - 1109,99 | -0,005 |
| 4-1 | - 262,08 | -366,63 | -0,502 |
| Всего | 0 | 0 | 0 |
3 Определение q , l , l *, ,
1)Процесс 1 – 2 (политропный).
q = 0,722(1,35-1,4)/(1,35-1)(811-363)=-47,21 кДж/кг.
l = 0,287/(1,35 – 1) (363 –811) = -366,26 кДж/кг.
l* = 1,35 0,287/(1,35 – 1)(363 – 811) = -495,94 кДж/кг.
= - 7
= 8
2)Процесс 2 – 3 (изохорный).
q = u =732,11 кДж/кг
l = 0
l*= - 0,104(50,37- 22,387) 102= - 291,02 кДж/кг
= 1
= 0
3) Процесс 3 – 4 (адиабатный).
q = 0
l = 0,287/(1,4-1)(1825-726) = 788,53 кДж/кг.
l* = - i = 1109,99 кДж/кг.
=
=
4)Процесс 4 – 1 (изохорный).
q = u = -262,08 кДж/кг
l = 0
l*= - 1,042(1- 2) 102= 104,2 кДж/кг
= 1
= 0
Таблица №3
| № процессов | q, кДж/кг | l, кДж/кг | l*, кДж/кг | , | , |
| 1 – 2 | -47,21 | -366,26 | -495,94 | -7 | 8 |
| 2 – 3 | 732,11 | 0 | -291,02 | 1 | 0 |
| 3 – 4 | 0 | 788,53 | 1109,99 | ||
| 4 - 1 | -262,08 | 0 | 104,2 | 1 | 0 |
| Всего | 422,82 | 422,27 | 427,23 | - | - |
4 Определение l ц, , P
lц = 422,8 кДж/кг
qподв =732,11 кДж/кг
=lц / qподв= 422,8/732,11 = 0,578 = 57,8 %
Pi=lц / Vmax - Vmin= 422,8103/(1,042- 0,104) = 0,451 МПа
5 Расчет промежуточных точек
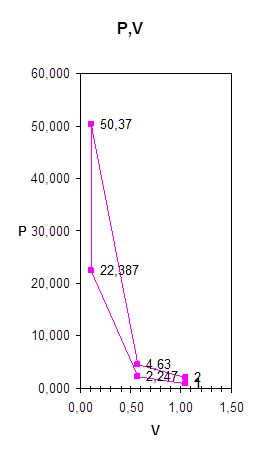
1.Для графика в P-V координатах:
а) по оси V
1.V1=(V1 + V2)/2=(1,042+0,104)/2=0,572
2.V2=(V3 + V4)/2=(1,042+0,104)/2=0,572
б) по оси Р
1.Р1=Р1*(V1/V1)n=1*105*(1,042/0,572)1,35=2,247*105
2.Р2=Р3*(V3/V2)к=50,37*105*(0,104/0,572)1,4=4,63*105
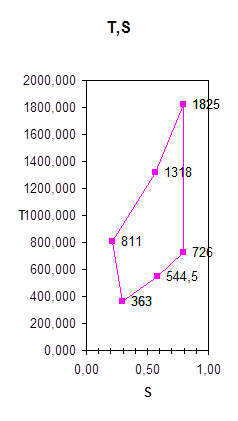
2.Для графика в T-S координатах:
а) по оси Т
1.Т1=(Т2+Т3)/2=(811+1825)/2=1318
2.Т2=(Т3+Т4)/2=(1825+726)/2=1275,5
3.Т3=(Т4+Т1)/2=(726+363)/2=544,5
б) по оси S:
а)2-3P1=P2*(T1/T2)=22,387*105*(1318/811)=36,38*105
б)3-4P2=P3*(T2/T3)= 50,37*105*(1275,5/1825)=35,20*105
в)4-1P3=P1*(T3/T1)= 1*105*(544,5/363)=1,5*105
1.S1=Cp*ln(T1/273)-R(P1/1,013)=1,01*ln(1318/273)-0,287* *ln(36,38/1,013)= 0,562
2.S2=Cp*ln(T2/273)-R(P2/1,013)=1,01*ln(1275,5/273)-0,287* *ln(35,20/1,013)= 0,659
3.S3=Cp*ln(T3/273)-R(P3/1,013)=1,01*ln(544,5/273)-0,287* *ln(1,5/1,013)= 0,585
Литература
1. Сборник задач по технической термодинамике /Т. И. Андрианова, Б. В. Дзампов, В. Н. Зубарев, С. А. Ремизов – М.: Энергия, 1971.
2. Ривкин С. Л. Термодинамические свойства газов. – М.: Энергия, 1973.
3. Кириллин В. А., Сычев В. В., Шейндлин А. Е. Техническая термодинамика. – М.: Энергия, 1976.
4. Ривкин С. Л., Александров А. А. Термодинамические свойства воды и водяного пара. – М.: Энергия, 1975.